



选项 | 物质(括号内为杂质) | 去除杂质的方法 |
A | NaCl(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
B | CaO(CaCO3) | 加水、过滤 |
C | Fe(Zn) | 加过量FeSO4溶液、过滤 |
D | H2SO4(HNO3) | 加Ba(NO3)2溶液、过滤 |
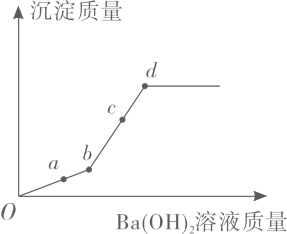

【定性探究】小科取其中一瓶氢氧化钠样品进行实验,实验过程及现象如图甲。

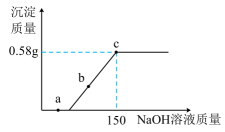
【定量实验】小丽取另—瓶氢氧化钠样品进行定量实验。将瓶中样品全部倒入烧杯中,加水充分溶解。逐滴加入溶质质量分数为7.3%的稀盐酸充分反应,当溶液的pH恰好为7时,所加稀盐酸的质量为100克。


【查阅资料】部分氢氧化物形成沉淀时所对应的溶液pH,如表所示。
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀时溶液的pH | 1.9 | 4.2 | 9.1 |
| 完全沉淀时溶液的pH | 3.2 | 6.7 | 11.1 |
①氯化钠 ②碳酸钠 ③碳酸钡 ④稀盐酸
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小红对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一: Na2CO3 猜想二: NaOH和 Na2CO3
【实验设计】为了验证上述猜想哪个正确,小红设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色的变化可以得出结论。小敏认为小红的实验方案不合理,理由是 。
【实验与结论】小敏另外设计实验方案并进行了探究,请你帮她完成下面的实验报告:
|
实验步骤 |
实验现象 |
结论 |
|
步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液并振荡 |
有白色沉淀产生 |
猜想一正确 |
|
步骤2:将步骤1试管中的混合物过滤,。 |
|

【查阅资料】煤炭主要成分是碳,遇水或氧气不足时会生成有毒气体一氧化碳。
【建立猜想】同学们对生成的气体成分做了以下猜想:
猜想1:有CO、CO2
猜想2:有CO、H2
猜想3:有CO、CO2和 H2
猜想4:有CO、H2、CO2和 H2O
【初步分析】

如何连接组装实验装置,同学们意见不一。某同学按照C→A→C→B→B→D→B→C的顺序连接装置,将生成的气体通过该装置,请评价该方案是否可行,理由是

①该实验中判断氢气存在的关键现象是。
②在该实验探究过程中,G装置的作用是。