 陶瓷花瓶
B .
陶瓷花瓶
B .  纯棉帽子
C .
纯棉帽子
C .  黄金首饰
D .
黄金首饰
D .  塑料油瓶
塑料油瓶

 B . 收集的氧气验满
B . 收集的氧气验满  C . 比较锌和铁的活泼性
C . 比较锌和铁的活泼性  D . 测定空气中氧气含量
D . 测定空气中氧气含量 
选项 | 需要鉴别的物质 | 鉴别方法 |
A | 稀硫酸、氯化钠溶液、氢氧化钠溶液 | 滴加紫色石蕊溶液 |
B | 碳酸钠、硫酸铜、碳酸钙 | 加入足量的水 |
C | 一氧化碳、氢气、氧气 | 用燃着的木条点燃 |
D | 铁粉、木炭粉、氧化铜粉末 | 加入足量的稀硫酸 |

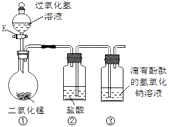
|
|
|
|
A.向一定质量的AgNO3和Cu(NO3)2的混合溶液中不断加入铁粉 | B.将浓硫酸露置在空气中 | C. 在恒温条件下,将饱和的NaCl溶液蒸发适量水 | D.向一定质量的饱和石灰水中加入生石灰 |
23-A | 23-B |
普通玻璃是Na2SiO3、CaSiO3、SiO2等物质经熔化后熔合在一起所得,玻璃是(填“纯净物”或“混合物”);将纯碱、石英砂(SiO2)、石灰石等原料粉碎,按照适当的比例混合后,经过高温加热制得普通玻璃,同时会产生CO2。写出纯碱与石英砂发生反应的化学方程式。 | 紫砂茶具属于陶瓷器。紫砂是指矿石成分中二氧化硅、氧化铝及氧化铁含量较高的陶土。SiO2、Al2O3、Fe2O3都属于(填“单质”或“氧化物”);某地紫砂中含氧化铝和氧化铁的质量分数分别为17%和3%。 请选择Al2O3、Fe2O3中的一种物质,计算该物质中所含各元素的质量比。 |



一般用含有淀粉的原料酿制白酒,但不同的原料酿制出的白酒风味各不相同。我国的白酒生产中,传统的固态发酵法的制作过程主要有以下步骤: 原料粉碎——配料(原料混合)——蒸煮糊化——冷却——拌醅——入窖发酵——蒸酒(蒸馏)。
白酒的香气来源于三方面。首先是原材料中带入,像高粱就可分解为丁香酸,进而增加白酒的芳香;其次是在发酵过程中,产生的多种具有特殊香气的有机物;还有就是在发酵、蒸馏或贮存过程中有机物发生化学反应生成的香味物质。
白酒的度数是指酒中所含乙醇(酒精)的体积百分比。某白酒每100毫升中乙醇含量为40毫升,这种酒的度数就是40°。液体体积是随环境温度的变化而变化,我国规定在温度为20℃时检测,也就是20℃时,100mL酒中含有乙醇的体积数(mL)为该酒的度数。
粮食酿造的白酒中含有醛类物质,而由乙醇(或甲醇)勾兑的假酒不含醛类物质。因此,可以通过对醛类物质的检测来鉴别真假白酒。
下面是真假白酒的对比实验。
在3支洁净试管中,先分别加入5mL真酒,再分别加入不同体积的质量分数为40%的NaOH溶液,加热。观察并记录实验现象。将真酒替换为假酒,重复上述实验。
实验记录如下:
40%NaOH溶液体积/mL | 1.0 | 2.0 | 3.0 |
真酒 | 无 | 浅黄 | 黄 |
假酒 | 无 | 无 | 无 |
依据文章内容回答下列问题。


①该反应的化学方程式为。
②关于铜作为催化剂,下列说法正确的是(填字母序号)。
A.不加入铜,该反应就不能进行
B.铜可以作为任何化学反应的催化剂
C.加入铜的目的是为了提高该反应的速率

写出上图中反应I的化学方程式;符合上图转化关系的物质丙的化学式是,物质已具有的一种用途是。
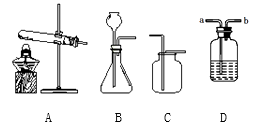


制备氯化氢。加热浓硫酸与氯化钠固体发生复分解反应制氯化氢气体,该反应的化学方程式是。
|
实验操作 |
实验现象 |
|
|
①红色物质附着于铝片表面 ②铝片表面逸出大量无色气体,放出大量的热 ③烧杯底部出现红色沉淀和白色沉淀 |
乙同学通过查阅资料认为白色沉淀可能是氯化亚铜(CuCl)。
CuCl中铜元素的化合价是。
①CuCl可与浓氨水反应生成无色的Cu(NH3)2+和Cl-。
②Cu(NH3)2+在空气中易被氧化变为蓝色;Cl-可与硝酸银溶液反应,产生白色沉淀。
【进行实验】
①取烧杯底部的白色沉淀,充分洗涤;
②向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
③取其中一份无色溶液……
④将另一份无色溶液放置于空气中……
以上步骤③的实验方案是;步骤④的现象是。
【得出结论】通过实验可以确定,该白色固体是CuCl。
丙同学猜测:可能是Cu与CuCl2溶液反应生成了CuCl。
丙同学为了验证猜想,取Cu粉与15% CuCl2溶液混合,无白色沉淀产生。
丙通过分析Al与CuCl2溶液反应的实验现象,改进了实验,证明了Cu与CuCl2溶液反应生成了CuCl,改进之处是。