| 甲的质量/g | 乙的质量/g | 丙的质量/g | 丁的质量/g | |
| 反应前 | 64 | 10 | 1 | 16 |
| t时刻 | 32 | A | ||
| 反应后 | 0 | 54 | b | 0 |
实验方法是:均匀称取七份样品分别和稀盐酸反应(CaCO3+2HCl=CaCl2+H2O+CO2↑),用电子天平及有关装置进行实验,实验数据记录如下表。(其他物质既不溶于水也不跟酸反应)
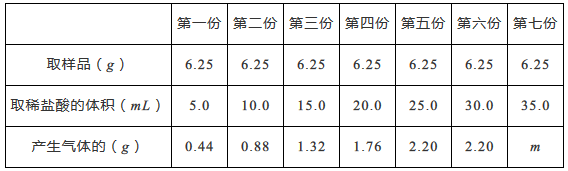
通过对数据的分析和比较,回答下列有关问题

| 组别 | 1 | 2 | 3 | 4 | 5 |
| 加入样品的质量/克 | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/克 | 10 | 20 | 30 | 40 | 50 |
| 充分反应后生成气体的质量/克 | 0.44 | 0.88 | 1.32 | 1.54 | 1.54 |
|
实验组别 |
1 |
2 |
3 |
4 |
|
加样品的质量(克) |
5 |
10 |
15 |
20 |
|
生成CO2的质量(克) |
1.76 |
M |
4.4 |
4.4 |

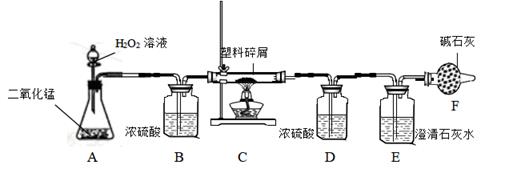
A、若反应时间过短,会因反应不充分,使测量结果不准。
B、若反应一段时间后,排出反应装置内原有空气再连接收集气体装置,会使结果更准确

|
烧杯A |
烧杯B |
烧杯C |
烧杯D |
烧杯E |
|
|
加入贝壳样品的质量/g |
8 |
8 |
8 |
8 |
8 |
|
加入稀盐酸的质量/g |
10 |
20 |
30 |
40 |
50 |
|
充分反应后生成气体的质量/g |
0.77 |
1.54 |
x |
3.08 |
3.08 |
Na2CO3+HCl=NaHCO3+NaCl,然后才发生反应:
NaHCO3+HCl=NaCl+CO2↑+H2O。
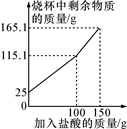
已知:该温度下CO2密度为1.98g/L,实验测得产生的CO2的与加入稀盐酸的数据如图。

②原样品中Na2CO3和NaHCO3的质量各是多少?
|
烧杯 |
大理石 |
稀盐酸 |
反应后烧杯总质量 |
|
|
质量(克) |
90 |
9 |
50 |
145.7 |
|
物质 |
第一份 |
第二份 |
第三份 |
第四份 |
|
反应前A的质量(克) |
11 |
8 |
a |
|
|
反应前B的质量(克) |
1 |
4 |
b |
|
|
反应后生成C的质量(克) |
5 |
10 |
7.5 |
|
实验次数 |
第一次 |
第二次 |
第三次 |
|
剩余固体的质量/克 |
10 |
5 |
5 |
求:

| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 粉末状大理石生成的CO2质量/克 | 0 | 1.45 | 1.75 | 1.96 | 2.10 | 2.16 | 2.19 | 2.20 | 2.20 | 2.20 |
| 块状大理石生成的CO2质量/克 | O | 0.45 | 0.80 | 1.10 | 1.36 | 1.60 | 1.81 | 1.98 | 2.11 | 2.18 |

|
样品编号 |
① |
② |
③ |
④ |
|
稀盐酸的质量 |
25g |
50g |
m |
150g |
|
剩余固体的质量 |
7.5g |
5g |
2g |
2g |
分析题中有关信息和图表,回答下列问题:

|
时间(分钟) |
0 |
0.5 |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
|
电子天平示数(克) |
160 |
158.2 |
157 |
156.4 |
156.04 |
156.04 |
156.04 |


|
第一次 |
第二次 |
第三次 |
第四次 |
|
|
加入稀盐酸的质量(g) |
20 |
20 |
20 |
20 |
|
烧杯中剩余物的质量(g) |
30.5 |
48.5 |
68.1 |
88.1 |
