
 B . 向二氧化锰中加入过氧化氢溶液
B . 向二氧化锰中加入过氧化氢溶液  C . 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液
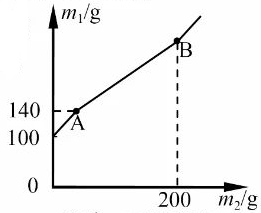
C . 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液 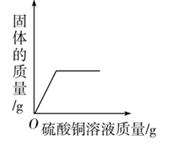 D . 等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
D . 等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应 
①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5克白色沉淀。
②在沉淀中加入过量稀硝酸,仍有3克白色沉淀。
③在滤液中滴加AgNO3溶液,产生白色沉淀。则该固体中一定含有( )
 B . 向一定质量的稀硫酸中滴加水
B . 向一定质量的稀硫酸中滴加水  C . 向氯化铁和盐酸的混合溶液中滴加氢氧化钠溶液至过量
C . 向氯化铁和盐酸的混合溶液中滴加氢氧化钠溶液至过量  D . 高温煅烧一定质量的石灰石
D . 高温煅烧一定质量的石灰石 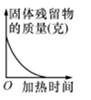
 B . 向氢氧化钠和硝酸钡的混合溶液中逐滴加入稀硫酸
B . 向氢氧化钠和硝酸钡的混合溶液中逐滴加入稀硫酸  C . 在一定质量的稀硫酸中,逐渐加入氢氧化钡溶液
C . 在一定质量的稀硫酸中,逐渐加入氢氧化钡溶液 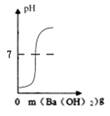 D . 向一定温度下的饱和氢氧化钙溶液中加入氧化钙
D . 向一定温度下的饱和氢氧化钙溶液中加入氧化钙 
①将甲溶液分别与其他三种溶液混合,都有白色沉淀生成;
②将乙溶液与丁溶液混合,有气泡产生;
③向丙溶液中滴入AgNO3溶液,出现白色沉淀,加稀硝酸后,沉淀不消失;
分析实验得到的以下结论中错误的是( )
 B .
B .  C .
C .  D .
D . 
 B . 在NaOH溶液中加入CaCO3 , 然后向其中逐滴加入稀盐酸
B . 在NaOH溶液中加入CaCO3 , 然后向其中逐滴加入稀盐酸  C . 在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸
C . 在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸  D . 在NaOH溶液中加入Ba(NO3)2 , 溶液,然后向其中逐滴加入稀硫酸
D . 在NaOH溶液中加入Ba(NO3)2 , 溶液,然后向其中逐滴加入稀硫酸 

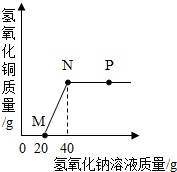
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示。
Ⅱ.取少量B点时的溶液于试管中,滴加酚酞试液,溶液不变色。
Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示。
下列说法正确的是( )

①红磷在密闭容器中燃烧
②盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液
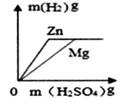
③等质量、等质量分数的稀硫酸中分别加入过量锌粉和铁粉
④一定质量的稀盐酸中,逐滴加入与稀盐酸等质量、等质量分数的氢氧化钠溶液
步骤①:取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解。
步骤②:接着向烧杯中加入足量稀硝酸并不断搅拌,此时固体质量变化如图。
下列说法正确的是( )

AlCl3+ 3NaOH = Al(OH)3↓+ 3NaCl ,Al(OH)3 + NaOH = NaAlO2 + 2H2O ,NaAlO2易溶于水。
下列图像正确的是( )
 B .
B .  C .
C .  D .
D . 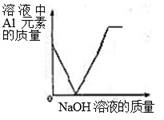



请回答下列问题:
①取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀和滤液.
②向所得固体中加入足量稀硝酸,白色沉淀全部溶解,且有气泡产生.
③向所得滤液中加入稀硫酸,有白色沉淀生成。
据此推断,
[查阅资料]①浓硫酸既可吸收水,也可吸收氨气
②NH3+HCl=NH4Cl
③2NH3+3CuO 3Cu+N2+3H2O

[实验分析]
B装置是利用了浓硫酸具有性。
[实验结果]原混合气体中各物质的组成情况是。(算出质量)

II.向甲中加入石灰石,乙中加入碳酸钠溶液,连接装置。
III.打开K1 , 用注射器向甲中注入稀盐酸,直至液面浸没下端导管口。
IV.通过K1上方导管收集气体(收集装置略去)。
V.打开K2、K3 , 关闭K1 , 最终观察到乙中溶液变浑浊,停止实验。
甲中发生的反应方程式为;乙中液体变浑浊的方程式。
猜想一.没有别的溶质 猜想二.还有氯化钙
猜想三.还有氯化氢、氯化钙 猜想四.还有碳酸钠
其中,猜想不成立,理由是。
为证明究竟哪种猜想正确,可以选择下列试剂中的(填字母)。
A.稀盐酸、碳酸钾溶液 B.碳酸钠溶液、氢氧化钡溶液
C.硝酸银溶液、稀硝酸 D.二氧化碳、稀盐酸
Na2CO3+2HCl==2NaCl+H2O+CO2↑ NaOH+HCl==NaCl+H2O
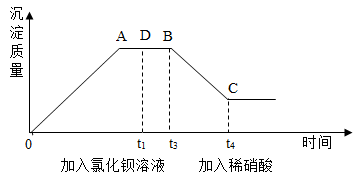
实验数据如图所示。试分析计算回答;

 B .
B .  C .
C .  D .
D . 

①在锥形瓶中加入质量为 m 的海螵蛸粉末,向分液漏斗中加入稀盐酸。在烧杯中加入足量氢氧化钠溶液,并称量烧杯及氢氧化钠溶液总质量 m1。
②先打开止水夹,再打开分液漏斗活塞,滴加盐酸并及时关闭活塞。完全反应后, 再次称量烧杯及其中液体的总质量 m2
方案一:样品 测定生成CO2的质量。

方案二:样品 测定剩余固体质量。
具体操作步骤如下:
①取一只洁净的坩埚,称得质量为21.2g,再向其中加入样品,称得总质量为41.2g;
②加热盛有样品的坩埚;
③将坩埚充分冷却,称量坩埚和剩余固体的质量;
④多次重复步骤②和③至恒重,称得坩埚和剩余固体的总质量为35.0g。
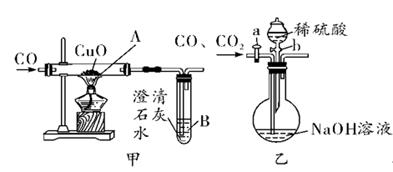
【查阅资料】:①氧化铜经一氧化碳还原不仅能生成铜,还可能生成中间产物氧化亚铜(Cu2O);②Cu2O是不溶于水的红色固体,能与酸发生反应,生成Cu2+和Cu。
【提出猜想】:氧化铜经一氧化碳还原所得到的红色固体中除Cu外还可能含有Cu2O。
【进行实验】:小明设计了一个最简单的实验方案:
|
实验步骤 |
取少量该红色固体放入盛有的试管中,振荡 |
|
实验现象及结论 |
|
Na2CO3+CaCl2=2NaCl+CaCO3↓。现有100克碳酸钠溶液,将150克氯化钙溶液分4次
加入,充分反应,测量所得数据如下表所示:
|
次数 |
第1次 |
第2次 |
第3次 |
第4次 |
|
加入氯化钙溶液的质量/克 |
40 |
40 |
40 |
30 |
|
所得溶液的总质量/克 |
134 |
168 |
202 |
232 |
| 组别 | 样品质量(克) | 加入稀硫酸体积(毫升) | 剩余固体质量(克) |
| 1 | 6.0 | 20.0 | 3.2 |
| 2 | 6.0 | 30.0 | 1.8 |
| 3 | 6.0 | 40.0 | 0.4 |
| 4 | 6.0 | 50.0 | 0.4 |

据图回答:
