






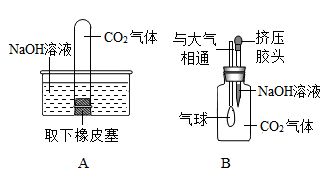
为验证性质④,他选择了二氧化碳与其反应,为探究两者是否发生了化学反应,小李设计了如图所示的A、B实验进行验证。实验现象为:A中试管内液面上升,B中。
李莉提出质疑,她认为A实验不严谨,应做一个对比实验:。





当观察到现象时,说明过滤 1 可以进行了。在该方案中,稀盐酸的作用是。

①酸碱电离理论:凡在水溶液中电离出的阳离子全部都是H+的物质叫酸;电离出的阴离子全部都是OH-的物质叫碱。
②酸碱溶剂理论:凡在溶剂中产生该溶剂特征阳离子的溶质叫酸;产生该溶剂特征阴离子的溶质叫碱。例如,液氨可电离出NH4+和NH2-两种离子,当液氨作为溶剂时,NH4+为特征阳离子,NH2-为特征阴离子。
③酸碱质子理论:凡能够给出质子(H+)的都是酸;凡能够接受质子(H+)的物质都是碱。
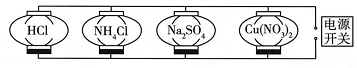
电源开关处的物质是(填化学式),Na2SO4 , 处对应的现象是。






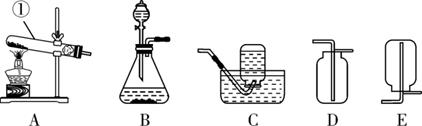
①金属表面除锈②制造药物氯化锌
③除去NaCl中的少口NaOH④实验室制取CO2。
①  ②
② 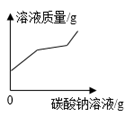 ③
③  ④。
④。 




A.氯化钡是一种有毒的重金属盐,使用时应注意安全
B.步骤②将滤渣进行水洗,既能提高氯化钡晶体的产率,又能减少 Ba2+对环境污染
C.可用重晶石(主要成分是 BaSO4)代替该实验流程中的毒重石,制备氯化钡晶体
D.滤液Ⅱ是不饱和溶液
