
| 反应时间/min | | |
| 0 | 0.30 | 0.60 |
| 20 | 0.10 | |
| 30 | 0.20 |
下列说法正确的是( )

| t/s | 0 | 3 | 6 | 12 | 24 |
| n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 |
下列有关说法正确的是( )

容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系能量的变化 | |||
CO | H2O | CO2 | H2 | ||
① | 1 | 4 | 0 | 0 | 放出热量:32.8 kJ |
② | 0 | 0 | 1 | 4 | 热量变化:Q |
下列说法中正确的是( )

| 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法正确的是( )

容器 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度 | ||
c(H2) | c(I2) | c(HI) | ||
Ⅰ(恒容) | 0.1 | 0.1 | 0 | c(I2)=0.07 mol·L-1 |
Ⅱ(恒压) | 0 | 0 | 0.6 | |
容器 | 温度/℃ | 物质的起始浓度/mol•L﹣1 | 物质的平衡浓度/mol•L﹣1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
①在相同条件下要想得到182kJ热量,加入各物质的物质的量可能是
A.2molCO和4molH2
B.2molCO、4molH2和1mol CH3OH(g)
C.4molCO和4molH2
D.4molCO和6molH2
②将1mol CO和2mol H2充入一密闭容器中,保持恒温恒压时进行反应,达到平衡时,测得CO的转化率为20%。若在相同条件下,起始时在该容器中充入1mol CH3OH(g),反应达到平衡时的热量变化是 (填“吸收”或“放出”) kJ热量。
①在题干条件下,说明该反应已经达到平衡状态的有(填序号)。
A.消耗0.1molA的同时生成0.1molC
B.容器中气体的压强不随时间而变化
C.容器中气体的密度不随时间而变化
D.A的转化率为50%
②保持容器温度和容积不变,若开始时向容器中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1、Q2与q的数值关系正确的是(填序号)。
A.Q1+Q2=q B.Q1+2Q2<q C.Q1+2Q2>q D.Q1+Q2<q
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入amolA气体,重新达平衡后,B气体的转化率为75%,则a=。

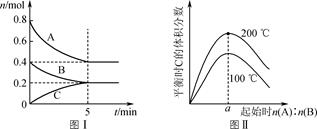
①A、B、C三点的平衡常数KA、KB、KC的大小关系为。
②若达到平衡状态A时,容器的体积为8L,则在平衡状态B时容器的体积为L。


已知:2H2(g)+O2(g)=2H2O (g)△H1= -483.6 kJ•mo1-1;
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H2=-1352.86 kJ•mol-1
△H =。

①该反应适宜选用的催化剂为(填“X'”或 “Y”)。
②T1K时,a点对应容器在0~5 min内的平均反应速率v(H2)=;b、c点对应状态下反应物的有效碰撞几率bc(填“>”“<”或“=”),原因为。
③T2K时,若反应前容器内的压强为p, 则该温度下反应的平衡常数KP=。 (KP为用分压表示的平衡常数)。

四个过渡态中对反应速率影响最大的是,理由为;该步骤的化学方程式为。
①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②CO(g)+2H2(g) CH3OH(g) ΔH2
③2CH4(g)+O2(g) 2CH3OH(g) ΔH3=-251.0 kJ·mol-1

①该反应自发进行的条件是(填“低温”、“高温”或“任意温度”)
②506 K时,反应平衡时H2的转化率为;压强:p1(填“>”“<”或“=”)p2。
③反应速率:N点v正(CO)(填“>”“<”或“=”)M点v逆(CO)。
④若压强为p1、在1L恒容密闭容器中进行上述反应(起始投料不变),在不同温度下上述反应的平衡常数的对数(lg K)如图所示。则温度为506 K时,平衡常数K=(保留三位小数),B、C、D、E四点中能正确表示该反应的lg K与T的关系的点为。

已知:Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g) ΔH 1=+489.0 kJ·mol-1
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为。

②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是。
a.容器中压强不变 b.H2的体积分数不变 c.c(H2)=3c(CH3OH) d.容器中密度不变 e.2个C=O断裂的同时有3个H-H断裂
