



| 选项 | 所用试剂 | 现象和结论 |
| A | 硫酸铜溶液 | 出现蓝色沉淀,则氢氧化钠过量 |
| B | 石蕊溶液 | 呈紫色,则恰好完全反应 |
| C | 锌粒 | 有气泡产生,则硫酸过量 |
| D | 氯化钡溶液 | 出现白色沉淀,则硫酸过量 |
 B . 稀释浓硫酸
B . 稀释浓硫酸 C . .酸碱反应
C . .酸碱反应 D . 蒸发Na2SO4溶液
D . 蒸发Na2SO4溶液
| 实验方案 | 使用的试剂 | 判断的方法 |
| A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
| B | pH试纸 | 如果pH<7,表明盐酸已经过量 |
| C | 硝酸银溶液 | 如果有白色沉淀产生,表明盐酸已经过量 |
| D | 紫色石蕊试剂 | 如果溶液变成红色,表明盐酸已经过量 |
①人体胃酸主要成分是,胃酸过多我们可以利用酸能用碱中和性质,可以服用复方氢氧化铝来中和,中和反应的实质是。
②CO具有,所以高炉炼铁时能用它夺取铁矿石中的氧;又因为CO有,所以做实验时可以用酒精灯把尾气点燃来处理尾气。
③高锰酸钾加热能分解出氧气,所以实验室我们用它来制取氧气。高锰酸钾属于(选填“酸”、“碱”或“盐”),锰元素的化合价为。

A.Fe B.酚酞溶液 C.CuSO4 D.Ba(NO3)2

①小苏打治疗胃酸过多 ②熟石灰改良酸性土壤 ③硫酸与火碱反应


|
方案 |
方案一 |
方案二 |
|
实验操作 |
在反应后的溶液中滴加氯化钡溶液 |
在反应后的溶液中滴加紫色石蕊试液 |
|
实验现象 |
出现白色沉淀 |
溶液变红 |
|
实验结论 |
硫酸过量 |
硫酸过量 |
小白与同学讨论后,指出小明设计的实验方案中有一个方案不合理,请指出不合理的方案并说明理由:。
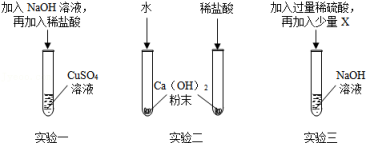
在实验1中,用滴管缓慢滴入稀盐酸,并不断搅拌。观察到现象时,证明了盐酸和 NaOH溶液发生了化学反应。
在实验2中,将稀盐酸全部注入试管中,立即固定活塞。观察到氢氧化钠固体全部消失,U形管的液面左低右高,部分同学由此认为氧氧化钠和盐酸发生了反应。但有的同学费同,他认为仍利用此装置,再补充一个实验才能达成实验2日的,实验时,针筒内需要的试剂及用量为。

实验3是醋酸与烧碱进行的三个实验,其中硅胶具有吸水性,吸水后由蓝色变红色。若醋酸与烧碱能反应,你能预测的实验现象是:。


|
反应时间(秒) |
0 |
25 |
50 |
75 |
100 |
125 |
150 |
175 |
200 |
|
滴入稀盐酸体积(毫升) |
0 |
4 |
8 |
12 |
16 |
20 |
24 |
28 |
32 |
|
pH |
13.2 |
13.0 |
12.7 |
12.4 |
12.1 |
7.0 |
2.0 |
1.6 |
1.3 |
|
温度(℃) |
36.9 |
37.5 |
38.0 |
38.5 |
38.8 |
39.2 |
39.0 |
38.8 |
38.6 |

①a的值是 ▲ ;
②求反应后溶液中溶质的质量分数。
