 B .
B .  C .
C .  D .
D . 


随时间变化的有关实验数据见下表:
时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
200℃ | 1.60 | 1.10 | 0.70 | 0.40 | 0.30 | 0.30 |
t℃ | 2.00 | 1.30 | 0.70 | 0.36 | 0.36 | 0.36 |
下列有关该反应的描述正确的是( )

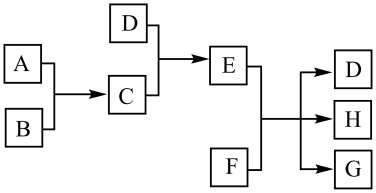
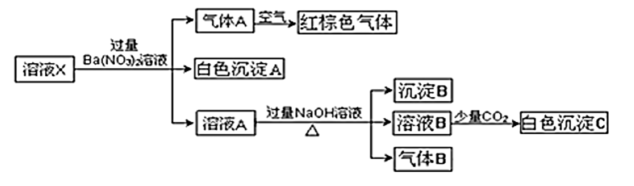
请回答下列问题:
①C的化学式是,D的电子式为。
②如何检验E溶液中阳离子?。
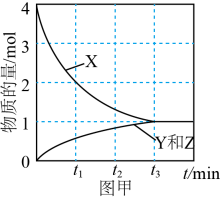

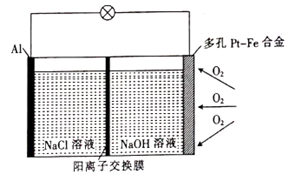
若原电池中生成单质S,其反应的离子方程式为。
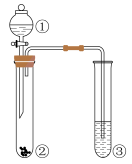
某小组同学欲探究NH3催化氧化反应,按下图装置进行实验.
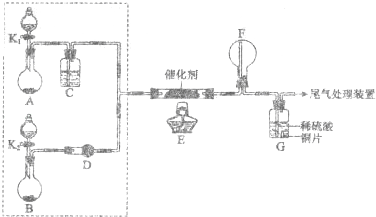
A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)NH3催化氧化的化学方程式是 ;
(2)装置B中产生气体的原因有(结合化学用语解释) ;
(3)甲乙两同学分别按上述装置进行实验.一段时间后,装置G中溶液都变成蓝色.
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是 ;
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式) ;
③用离子方程式解释装置G中溶液变成蓝色的原因: ;
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进.
①甲认为可调节K1和K2控制A、B装置中的产气量,应(填“增加”或“减少”) 装置A中的产气量,或(填“增加”或“减少”) 装置B中的产气量.
②乙认为可在装置E、F间增加一个装置,该装置可以是(填序号)

①该反应为(填“吸热”或“放热”)反应。
②为了探究化学能与热能的转化,某实验小组设计了图2实验装置,在甲试管里先加入适量铁片,再加入稀硫酸,U形管中可观察到的现象是。
③若要使该反应的反应速率加快,下列措施可行的是(填字母)。
A.铁片改为铁粉B.稀硫酸改为98%的浓硫酸C.升高温度

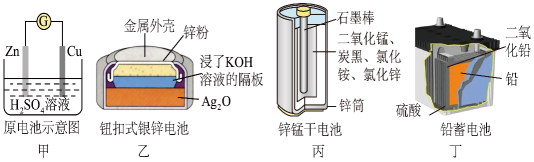
①铜为(填“正”或“负”)极;负极的电极反应式为。
②若该电池反应过程中共转移0.3 mol电子,则生成的H2在标准状况下的体积是L。
(1)下列反应属于吸热反应的是
A.C6H12O6(葡萄糖)+6O2═6CO2+6H2O
B.CH3COOH+KOH═CH3COOK+H2O
C.大多数化合反应
D.破坏生成物全部化学键所需能量小于破坏反应物全部化学键的能量
E.Ba(OH)2•8H2O晶体与NH4Cl晶体反应
F.金属与酸或水的反应
(2)在一定温度下的定容密闭容器中,发生反应:A(s)+2B(g)⇌C(g)+D(g),能表明反应已达平衡状态的是
A.混合气体的压强不变
B.混合气体的密度不变
C.单位时间内生成n molC的同时生成n mol D
D.气体总物质的量不变
E.A的物质的量不再变化
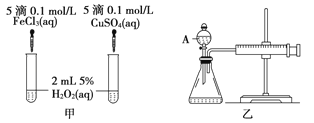
(3)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验.回答相关问题:
①定性分析:如图甲可通过观察 来定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.图中仪器A的名称为 ,实验中需要测量的数据是 .检查乙装置气密性的方法是 .