 B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
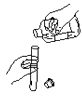 倾倒液体
B .
倾倒液体
B . 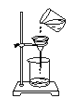 过滤
C .
过滤
C . 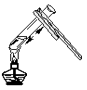 加热液体
D .
加热液体
D . 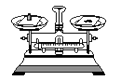 称量固体
称量固体
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别Cu和Fe3O4 | 观察颜色 |
| B | 除去CO2中少量的CO | 点燃 |
| C | 鉴别H2O 和H2O2溶液 | 分别取少量液体于试管中,加入MnO2 |
| D | 除去Cu粉中少量的Fe粉 | 用磁铁吸引 |

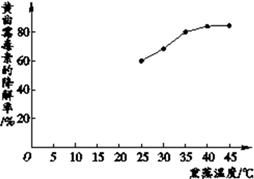

① 当温度为40 ℃和45 ℃时,降解率分别为84.34%和84.35%,考虑到经济性原则,应选取的最佳熏蒸温度为。
②在25 ℃~45 ℃的范围内,随着熏蒸温度的升高,黄曲霉毒素的降解率逐渐(填“增大”或“减小”)。

污染项目 | PM2.5 | PM10 | SO2 | CO | NO2 |
污染指数 | 69 | 95 | 9 | 0.8 | 42 |
①首要污染物是;其中会形成酸雨的是(填1种即可)。
② 上图为一款新型环保车,可通过360 °旋转的“大炮筒”向四周喷水,从而缓解极端恶劣天气给人带来的不适。分析这款环保车喷水的作用是。
资料:“湿垃圾”是指植物类和厨余类垃圾,由于含水量高、易腐坏更适于发酵制沼气和肥料等。除湿垃圾外的其他垃圾为“干垃圾”,经分拣后可分别被再利用。
![]() 纯金饰品
纯金饰品 ![]() 铁锅
铁锅 ![]() 通道县
通道县
A.导电性 B.导热性 C.黄金色有光泽
② 再举出1种“低碳”的生活方式:。

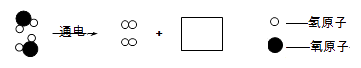
① 活性炭的主要作用是。
② 离子交换树脂能去除原水中的钙离子,钙离子的符号是。
| A | B |
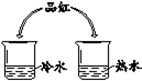 | 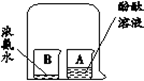 |
| 从微粒角度解释: ①品红在水中扩散的原因是。 ②品红在热水中扩散速度快,其原因是。 | ①实验现象是。 ②实验结论是。 |

| 实验装置 | 【实验1】制取O2 | 【实验2】用NaOH溶液除去 O2中混有的CO2 |
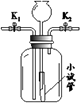 | I.广口瓶中放入少量MnO2 II.打开K2 , 从长颈漏斗加入H2O2溶液至溢出小试管 | I.打开K1、K2 , 从长颈漏斗加入足量NaOH溶液至瓶中液面高于左侧导管口且低于小试管口 II. …… |
①II中操作是:从(填“左”或“右”)侧导气管通入混合气体。
②除去CO2 的反应如下,补全该反应的化学方程式:2NaOH + CO2 = Na2CO3 +
③实验过程中,当通入气体的流速突然变大时,小试管可以防止广口瓶中大量液体从长颈漏斗上口溢出,其原因是。
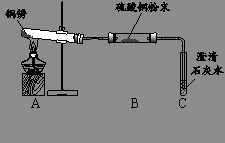
【提出猜想】根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
【进行实验】实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面 有绿色物质 | 无明显现象 | 无明显现象 |
【解释与结论】
实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是。
结合上述实验,你对保存铜制品的建议是。