
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | 甲 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 |
乙 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | |
丙 | 13.3 | 31.6 | 63.9 | 110 | 169 | |


温度/℃ | 0 | 10 | 20 | 30 |
NH4HCO3溶解度(g/100g水) | 11.9 | 15.8 | 21.0 | 27.0 |
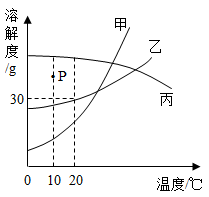

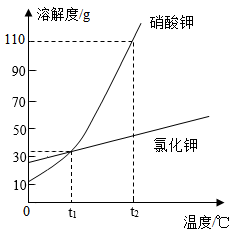
结合硝酸钾在不同温度下的溶解度,判断下列说法错误的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 |
KNO3溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |

温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |



|
KNO3和KCl在不同温度时的溶解度表 |
|||||||||
|
温度/℃ |
0 |
T1 |
20 |
T2 |
40 |
60 |
80 |
100 |
|
|
溶解度/g |
KNO3 |
13.3 |
25.0 |
31.6 |
35.1 |
63.9 |
110 |
169 |
246 |
|
KCl |
27.6 |
31.8 |
34.0 |
35.1 |
40.0 |
45.5 |
51.1 |
56.7 |
|
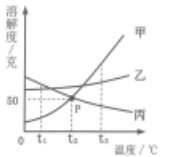
下列说法正确的是( )



温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
NaCl的溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
NH4Cl的溶解度/g | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |

温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | 氯化钾 | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 |
次氯酸钠 | 22.7 | 26.7 | 34.8 | 50.0 | 52.4 | 56.5 | |
①0℃时,100g水里最多只能溶解g氯化钾。
②30℃时,将30g次氯酸钠加入到装有50g水的烧杯中,充分溶解后,所得溶液的质量是g。将此溶液恒温蒸发10g水,烧杯中固体的质量为g。
③50℃时,将氯化钾和次氯酸钠的饱和溶液各100g分别降温至20℃,两溶液中溶质的质量大小关系是:氯化钾次氯酸钠(填“大于”“等于”或“小于”)。

温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |

A.两种溶液中溶剂的质量相等
B.两种溶液中溶质质量分数相等
C.t℃大于20℃



据此分析,x=,mgNaCl不饱和溶液中水的质量为g。

I.上述步骤的正确顺序为(填序号)。
Ⅱ.溶解时玻璃棒的作用为。