

| 序号 | 物质 | 性质 | 用途 |
| A | 稀盐酸 | 能与金属氧化物反应 | 金属除锈 |
| B | 氢氧化钙 | 能与二氧化碳反应 | 改良酸性土壤 |
| C | 碳酸钙 | 形成的岩石质地坚硬 | 做建筑材料 |
| D | 氯化钠 | 具有杀菌作用 | 清洗伤口 |
 向硫酸和硫酸铜混合溶液中逐滴加入一定溶质质量分数的氢氧化钠溶液
B .
向硫酸和硫酸铜混合溶液中逐滴加入一定溶质质量分数的氢氧化钠溶液
B . 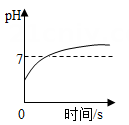 向一定质量的稀盐酸中逐滴加入等质量、等质量分数的氢氧化钠溶液
C .
向一定质量的稀盐酸中逐滴加入等质量、等质量分数的氢氧化钠溶液
C .  高温煅烧一定质量的石灰石
D .
高温煅烧一定质量的石灰石
D .  向一定量的饱和氢氧化钙溶液中加少量氧化钙
向一定量的饱和氢氧化钙溶液中加少量氧化钙
 B .
B .  C .
C .  D .
D . 

| 选项 | 实验 | 现象 |
| A | 将氢氧化钠固体放在表面皿上,放置一会儿 | 固体受潮,逐渐溶解 |
| B | 向盛有氢氧化钠溶液的试管中滴入无色酚酞试液 | 溶液变红 |
| C | 向盛有氢氧化钠溶液的试管中滴加稀盐酸 | 有氯化钠生成 |
| D | 向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液 | 产生蓝色沉淀 |

| 实验步骤 | 实验现象 |
| ①将固体研磨成粉末状,加水搅拌 | 固体没有全部溶解 |
| ②取上层清液,滴加酚酞试液 | 溶液呈红色 |
| ③取不溶物,滴加稀盐酸 | 有气泡产生 |









探究一:氢氧化钠固体是否变质:兴趣小组同学取少量氢氧化钠固体样品于试管中,加适量水溶解,滴加稀盐酸,产生大量气泡。回同答下列问题:
【查阅资料】:
①碱石灰是NaOH和CaO的固体混合物,能吸收水和二氧化碳
②标准状况下,二氧化碳的密度ρ=1.977g/L
③碳酸钠溶液与氯化钙溶液能发生反应:Na2CO3+CaCl2=CaCO3+2NaCl
【设计实验】:甲、乙两兴趣小组同学分别称取2g氢氧化钠样品与足量稀盐酸反应,通过测定产生二氧化碳的量进行计算。甲小组同学设计了如图所示的方案一测定二氧化碳的质量。(注:不考虑稀盐酸中HCl气体的挥发)

【交流讨论】
乙小组同学认为方案一的C装置气管水面上应覆盖一层植物油,防止二氧化碳溶于水,由此提出了方案二,但甲小组同学认为方案二的装置也存在缺陷,会对实验结果产生影响。请你指出产生影响的原因:(写一点)。

“操作I”的名称是;
①小柠认为,料液中一定存在NaCl和NaOH,料液中一定有NaOH的原因是(用化学方程式表示)。
②小柠猜想,料液中还有可能存在Ca(OH)2或Na2CO3 , 于是进行了如下实验:
实验1:取少量上层清液放入试管中,滴加少量Na2CO3溶液,有白色沉淀。
实验2:取少量上层清液放入试管中,滴加过量稀盐酸,没有明显现象。
由此可以得出,该料液中除NaOH与NaCl外,还含有(填写化学式)
|
同学 |
甲 |
乙 |
丙 |
|
操作 |
各取一支相同规格的试管,在试管中加入一定量的待测溶液 |
||
|
滴入无色酚酞试液 |
加入足量的 ? |
加入足量的BaCl2溶液 |
|
|
现象 |
变红 |
产生气泡 |
产生白色沉淀 |
|
结论。 |
没变质 |
变质 |
变质 |

【提示:AlCl3+3NaOH=Al(OH)3↓+3NaClㅤㅤAl(OH)3+NaOH=NaAlO2+2H2O】
①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克;@向上述3个烧杯中分别加入3份质量不同的样品;
②充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据记录如下:
|
实验一 |
实验二 |
实验三 |
|
|
反应前稀盐酸+烧杯质量(克) |
150 |
150 |
150 |
|
反应前固体样品质量(克) |
4 |
8 |
12 |
|
反应后烧杯内物质+烧杯质量(克) |
m |
155.8 |
158.7 |
请回答下列有关问题:
|
成分:氢氧化钠固体、铝粉 |
|
净含量: 200克 |
|
注意事项:使用时要防明火 |
|
保存方法:密封 |
|
使用范围:毛发残渣等淤积物 |
I.取样品 40g,倒入容积为 200mL 的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量 m1。
II.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量 m2。
III.实验数据如表。
请根据以上信息求样品中铝的质量分数。
|
反应前总质量m1 |
反应后总质量m2 |
|
372.44g |
371.24g |

请根据有关信息回答问题。
|
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
第6次 |
|
|
加入盐酸的质量/g |
25 |
25 |
25 |
25 |
25 |
25 |
|
锥形瓶中物质的质量/g |
75 |
100 |
a |
150 |
172.8 |
197.8 |