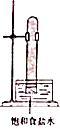
 B .
B . 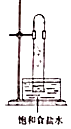 C .
C .  D .
D . 
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向待测液中依次滴入氯水和KSCN溶液 | 溶液变为红色 | 待测溶液中含有Fe2+ |
| B | 向浓度均为0.1mo/L的NaHCO3溶液和NaHSO3溶液中滴加几滴酚酞试剂 | 前者溶液变红,后者不变色 | NaHCO3水解,而NaHSO3不水解 |
| C | 向2支盛有2mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液 | 一只试管中产生黄色沉淀,另一支中无明显现象 | Ksp(AgI)<Ksp(AgCl) |
| D | 甲烷与氯气在光照下反应 | 产生混合气体能使湿润的石蕊试纸变红 | 生成的氯甲烷具有酸性 |



 苯乙烯在一定条件下可加聚反应,不可以发生取代反应
苯乙烯在一定条件下可加聚反应,不可以发生取代反应

查阅资料得:实验室制取甲烷常用的方法为无水醋酸钠 与氢氧化钠在二氧化锰作催化剂的条件下共热,产物中有少量的副产物丙酮
,丙酮可与水混溶。

A. 关闭、
关闭 B.
关闭、
打开
C. 打开、
打开 D.
打开、
关闭
|
实验前装置总质量/g |
D |
E |
F |
G |
|
实验后装置总质量/g |
180.0 |
277.8 |
311.5 |
301.0 |
|
实验前装置总质量/g |
177.2 |
279.6 |
312.6 |
301.0 |
若装置D中的氧化铜全部被还原成铜,则气球中收集到的由D中反应产生的气体在标准状况下的体积为L,此条件下,装置D中发生反应的化学方程式为。
制备
制备NH3(以浓氨水和生石灰为原料):。
下图所示分别为制备CH4和NH3并得到合适体积比混合气体的装置,根据上述原理选择合适的仪器并连接成装置,则连接顺序为a→e,→f(填接口标号)。装置E中的试剂为(选填“饱和食盐水”、“浓硫酸”或“四氯化碳”)。装置E相当于上述图1装置中的。


实验过程中,采用不同的催化剂,HCN的产率不同,下图所示分别为不同温度,不同催化剂条件下HCN、H2和N2的产率关系图。

由图可知,低温条件下最适宜的催化剂为,高温条件下,选择该催化剂不如另外两种作催化剂时HCN产率高的原因是。

②,反应类型为。
⑤,反应类型为。

①某同学预测的实验现象:a.气体最终变为无色;b.反应过程中,甲管活塞向内移动;c.甲管内壁有油珠;d.产生火花。其中正确的是(填字母,下同)。
②实验结束后,甲管中剩余气体最宜选用下列试剂吸收。
A.水 B.氢氧化钠溶液 C.硝酸银溶液 D.饱和食盐水
③反应结束后,将甲管中的物质推入盛有适量溶液的试管中,振荡后静置,可观察到,再向其中滴加几滴石蕊试液,又观察到。

①外电路电子移动方向为(填“a→b”或“b→a”)。
②a极的电极反应式为。
③若该燃料电池消耗空气5.6L(标准状况下),则理论上消耗甲烷mol(假设空气中体积分数为20%)。

①装置A、B中的实验现象分别为、
②写出甲烷与氯气反应生成一氯甲烷的化学方程式:
③若将2mol与一定量的
反应,得到等物质的量的4种取代物,则消耗
的物质的量为。


|
实验操作及现象 |
实验结论 |
|
|
A |
①在漫射日光条件下,试管内:、液面上方有形成、内壁上出现了油状液滴 |
③CH4与Cl2在条件下发生化学反应 |
|
B |
②迅速剥开黑纸,立即观察:试管内气体颜色为黄绿色 |
|
④1 mol甲烷与足量Cl2发生取代反应时,得到最多的产物是(填化学式)。

①②装置中可盛放的试剂是:①、②(填字母)。
A. 品红 B. NaOH溶液 C. 溴水 D. 酸性高锰酸钾溶液
通过探究,该同学得出结论:甲烷和乙烯在不同条件下均能与卤素反应。


| 实验操作及现象 | 实验结论 | |
| A | ①在漫射日光条件下,试管内:、液面上方有形成、内壁上出现了油状液滴 | ③CH4与Cl2在条件下发生化学反应 |
| B | ②迅速剥开黑纸,立即观察:试管内气体颜色为黄绿色 | |
④1 mol甲烷与足量Cl2发生取代反应时,得到最多的产物是(填化学式)。

①②装置中可盛放的试剂是:①、②(填字母)。
A. 品红 B. NaOH溶液 C. 溴水 D. 酸性高锰酸钾溶液
通过探究,该同学得出结论:甲烷和乙烯在不同条件下均能与卤素反应。
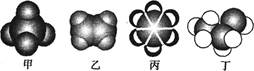
①能发生银镜反应的是(填序号,下同);
②能发生水解反应的是;
③具有酸性且能发生酯化反应的是;
④既能发生加成反应,又能发生加聚反应的是;
⑤能使酸性高锰酸钾褪色的是。

![]()