19.
(2022高二下·龙岩期中)
类石墨相氮化碳(g—C
3N
4)作为一种新型光催化材料,在光解水产氢等领域具有广阔的应用前景,研究表明,非金属掺杂(O、S等)能提高其光催化活性。g—C
3N
4 , 具有和石墨相似的层状结构,其中一种二维平面结构如图所示。下列关于g—C
3N
4 , 的说法错误的是( )

A . 基态C原子的成对电子数与未成对电子数之比为2:1
B . N、O、S的第一电离能(I1)大小为I1(N)>I1(O)>I1(S)
C . g—C3N4晶体中存在的微粒间作用力有非极性键、π键和范德华力
D . g—C3N4中,C原子的杂化轨道类型为sp2杂化,N原子的配位数为2和3






 (b)转化为
(b)转化为  (d),(b)可由对苯二酚
(d),(b)可由对苯二酚 


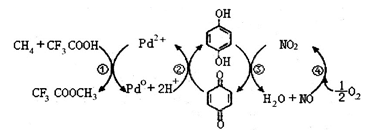
 均可以与浓溴水反应,且反应类型相同
均可以与浓溴水反应,且反应类型相同