










①该化合物分子中,模型为四面体或正四面体的非金属原子共有个。
②的电负性由大到小的顺序为。

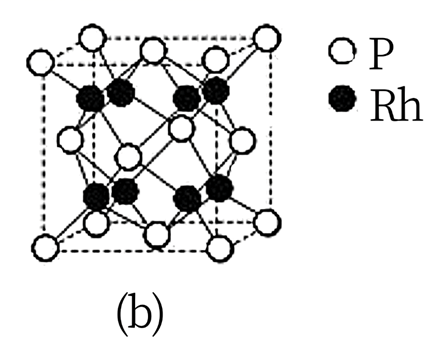
①的配位数为;晶体中
原子填充在
、
围成的四面体空隙中,则四面体空隙的占有率为。
②若晶胞底边的边长均为 , 高为
, 阿伏加德罗常数的值为
, 设晶体的最简式的式量为
, 则该晶体的密度为
(列出计算式)。

| 分数坐标 原子 | x | y | z |
| W | 0 | 0 | 0 |
| X | 0 | 0 | |
| Y | | | |
①B原子代表,C原子代表,与A原子距离最近的氧原子个数为。
②Z用分数坐标表示为。
③设阿伏加德罗常数的值为NA , 则La2CuO4的密度是g·cm-3(列出计算表达式)。


①晶胞中三价铁离子处于氧离子围成的(填空间结构)空隙。
②解释Fe3O4晶体能导电的原因。
③若晶胞的体对角线长为anm,则Fe3O4晶体的密度为g·cm-3(阿伏加德罗常数用NA表示)。

A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力

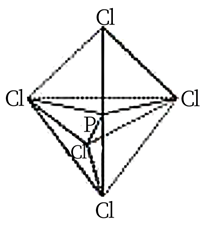
①[PCl4]+的空间构型为;
②五氯化磷既可溶于非极性溶剂CCl4 , 又可溶于极性溶剂硝基苯的原因是。

①其组成元素的电负性由小到大的排序为,其中碳原子的杂化方式为。
②甲脒比丙烷的熔点更高的原因是。

①该络合物可溶于四氯化碳,其晶体类型为。
②该络合物分子内不存在的微粒间作用力有。(选填序号)
a.σ键 b.π键 c.非极性键 d.配位健 e.离子键
①氨水中存在的化学键有 (填标号)。
A.极性键 B.非极性键 C.氢键 D.σ键 E.π键
②[Cu(NH3)4]CO3中配体是 ,所含元素中电负性最小的非金属元素是(填元素符号)。




 回答下列问题:
回答下列问题:
反应i.  +NH3
+NH3

反应ii,其反应类型是。
 、
、  制备扑炎痛
制备扑炎痛  的合成路线(其它试剂任选)。。
的合成路线(其它试剂任选)。。 +
+  +NaCl
+NaCl