



 D . Na晶体堆积方式
D . Na晶体堆积方式



 )表示的状态中,能量高的是①
)表示的状态中,能量高的是①





②图2为铜的某种氯化物晶胞示意图,该物质的化学式是。原子坐标参数可表示晶胞内部各原子的相对位置,上图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为。
③图示晶胞中C、D两原子核间距为298 pm,阿伏加德罗常数的值为NA , 则该晶体密度为 g▪cm-3(列出计算式即可)。
 。
。 ①LiAlH4中三种元素的电负性从大到小的顺序为。
②  分子中碳原子的轨道杂化类型为,1mol该分子中含σ键的物质的量为。
分子中碳原子的轨道杂化类型为,1mol该分子中含σ键的物质的量为。
 图1
图1
 图2
图2

铜原子的第一电离能为kJ•mol-1;Cl-Cl键键能为kJ•mol-1;CuCl的晶格能为kJ•mol-1。

①青霉胺分子中S原子的轨道杂化类型为;
②硫化氢与氨气键角的大小:H2SNH3(填“>”或“<”)。
③第二周期元素中,第一电离能大于N的元素有(用元素符号表示)。
④该环状络合物无毒、易溶于水,可经尿液排出,请解释该化合物易溶于水的主要原因:。
①离子化合物M的化学式为;
②已知Cs和Cl两元素离子的半径大小相近,该晶体中两种离子联合组成何种形式的密堆积;
③若晶胞参数为anm,则这种晶体密度为g•cm-3(用含a、和NA的式子表示)。

回答下列问题:


写出一种与Q互为等电子体的离子。
________________(填字母)。


已知GaAs与GaN具有相同的晶胞结构,则二者晶体的类型均为,GaAs的熔点(填“高于”或“低于”)GaN。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1 , 原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA , 则GaAs晶胞中原子的体积占晶胞体积的百分率为。
含硼、氮、磷的化合物有许多重要用途,如:(CH3)3N、Cu3P、磷化硼等。回答下列问题:
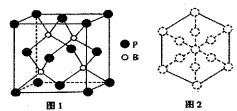
①在一个晶胞中磷原子的配位数为。
②已知磷化硼晶体的密度为ρg/cm3 , 阿伏加德罗常数为NA , 则B-P键长为pm。
③磷化硼晶胞沿着体对角线方向的投影如图2,请在答题卡上将表示B原子的圆圈涂黑。
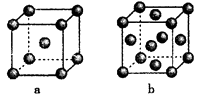
①铁采纳的是a堆积方式.铁原子的配位数为,该晶体中原子总体积占晶体体积的比值为(用含π的最简代数式表示)。
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为g·cm-3(用含有r、NA的最简代数式表示)。

a.离子键
b.配位键
c.非极性键
d. σ键



晶胞的棱长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,K与I间的最短距离为nm,与K紧邻的O的个数为。阿伏加德罗常数的值为6.02×1023 , 列式计算晶体的密度为g/cm3. (不必计算结果)

①组成该物质的元素中,电负性最大的是 (填元素名称)。
②M中,碳原子的杂化形式有种。
③M中,不含(填标号)。
a. π键 b. σ键 c.配位键 d.氢键 e.离子键

①4个微粒A、B、C、D中,属于氧原子的是。
②若A、B、C的原子坐标分别为A (0,0,0)、B (0.69a,0.69a,c)、c (a, a,c),则D的原子坐标为D (0.19a,,);钛氧键的键长d=(用代数式表示)。
 )分子中2号碳原子的杂化方式为;与CS2互为等电子体的阴离子是(写一种);CO32-的立体构型是。
)分子中2号碳原子的杂化方式为;与CS2互为等电子体的阴离子是(写一种);CO32-的立体构型是。

①一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是
②已知晶胞棱长a=5.64×10-10m.则该晶胞密度为ρ=。

①该晶体的化学式为。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于化合物(填“离子”、“共价”)。
③已知该晶体的密度为ρg·cm-3 , 阿伏加德罗常数为NA , 已知该晶体中Cu原子和M原子之间的最短距离为体对角线的1/4,则该晶体中Cu原子和M原子之间的最短距离为pm(写出计算列式)。
 B .
B .  C .
C .  D .
D . 


A.离子键B.配位键C.δ键D.范德华力

①该化合物的化学式为。
②该晶胞棱长为0.542 nm,则晶体的密度为(写出计算式即可,不计算结果)。
③该化合物难溶于水易溶于氨水,是因为可与氨形成易溶于水的配位化合物,若配位数是4,则络离子的化学式为。
该络离子在空气中易被氧化而导致溶液呈现色。


