①CuSO4+H2S=CuS↓+H2SO4
②11PH3+24CuSO4+12H2O=3H3PO4+24H2SO4+8Cu3P↓
下列分析错误的是( )
| A | B | C | D |
| | | | |
| 混合浓硫酸和乙醇 | 配制一定浓度的溶液 | 收集 | 证明乙炔可使溴水褪色 |


| 选项 | 实验操作和现象 | 结论 |
| A | 向FeCl2和KSCN的混合溶液中滴入硝酸酸化的AgNO3溶液,溶液变红 | 氧化性:Fe3+<Ag+ |
| B | 将蘸有浓氨水的玻璃棒靠近溶液X,有白烟产生 | 溶液X一定是浓盐酸 |
| C | 将电石与水反应产生的气体通入溴水,溴水褪色 | 生成的乙炔气体中含有H2S |
| D | 向碘水中加入等体积CCl4 , 振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |

| A | B | C | D |
| | | | |
| 收集 CO2 | 除去Cl2 中的 HCl | 配制 20.00mL0.1 mol∙L−1Na2CO3溶液 | 制取乙炔 |
| A | B | C | D |
| | | | |
| 分离乙醇与乙酸 | 模拟外加电流的阴极保护法 | 证明 | 证明乙炔可使溴水褪色 |
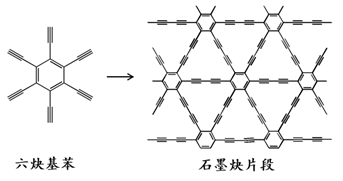
 模拟工业制纯碱
B .
模拟工业制纯碱
B .  甲烷的取代反应
C .
甲烷的取代反应
C .  实验室制乙炔
D .
实验室制乙炔
D .  除去氯气中的氯化氢
除去氯气中的氯化氢
| | | | |
| A.从溴水中提取溴 | B.验证乙炔的还原性 | C.制取并收集NO2 | D.实验室制取溴苯 |


 的单炔烃有( )
的单炔烃有( )

选项 | 操作 | 现象 | 结论 |
A | 向NaAlO2溶液中滴加NaHCO3溶液 | 产生白色沉淀 | AlO2-结合H+的能力比CO32-强 |
B | 蘸有浓氨水的玻璃捧靠近X | 有白烟产生 | X —定是浓盐酸 |
C | 将气体分别通入溴水和酸性高锰酸钾溶液中 | 两溶液均褪色 | 该气体一定是乙烯 |
D | 炭粉中加入浓硫酸并加热,导出的气体通入BaCl2溶液中 | 有白色沉淀产生 | 有SO2和CO2产生 |
实验目的 | A.探究铁钉发生析氢腐蚀 | B.验证溴乙烷发生消去反应 | C.对比Fe3+与Cu2+的氧化能力强弱 | D.探究乙炔的性质 |
实验方案 |
|
|
|
|
反应路线Ⅰ:
反应路线Ⅱ:
已知以下信息:
①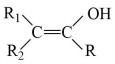
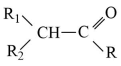
 (R、R1、R2为H或烃基)
(R、R1、R2为H或烃基)
②![]() +2ROH
+2ROH +H2O
+H2O
 有多种同分异构体,写出两种符合下列条件的同分异构体的结构简式。
有多种同分异构体,写出两种符合下列条件的同分异构体的结构简式。
a.链状结构
b.能发生水解
c.含有三种化学环境不同的氢原子
 是制备氯丁橡胶的原料,请设计以CH2=CH-CH=CH2原料制备
是制备氯丁橡胶的原料,请设计以CH2=CH-CH=CH2原料制备 的合成路线(用流程图表示,无机试剂、有机溶剂任选)。
的合成路线(用流程图表示,无机试剂、有机溶剂任选)。
(合成路线常用的表示方式为:AB……
目标产物)
①苯环上有四个取代基,其中有两个取代基相同;
②含有碳碳三键和酯基,且处于对位;
③能发生银镜反应、水解反应,与溶液能发生显色反应。
其中核磁共振氢谱峰面积之比为2∶2∶2∶1∶1的结构简式为(任写出其中一种)。
 为原料制备
为原料制备 的合成路线流程图:(其他无机试剂任用)。
的合成路线流程图:(其他无机试剂任用)。
a.含酯基,不含醚键![]() b.1mol该有机物与足量银氨溶液反应,生成4mol Ag
b.1mol该有机物与足量银氨溶液反应,生成4mol Ag


已知∶①E 与 Br2恰好按物质的量比1∶1 反应
②
回答下列问题∶

| 序号 | 气体 | 反应原理 | A中试剂 |
| ① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 |
|
| ② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是。 | NaOH溶液 |
| ③ | 乙炔 | 电石与饱和食盐水反应 |
|
|
试管编号 |
① |
② |
③ |
|
实验操作 |
| | |
| 实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
试管①中反应的化学方程式是;
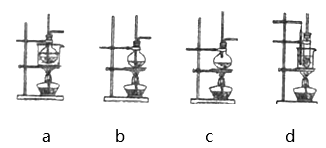
a 吸水性 b 脱水性 c 强氧化性 d 酸性
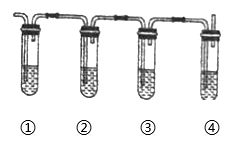
有同学设计下列实验确认上述混合气体中有乙烯和二氧化硫。
上图中①、②、③、④装置盛放的试剂分别是(根据需要进行选择,填标号):
①,②,③,④。
A 品红溶液 B NaOH溶液 C 浓硫酸 D 酸性高锰酸钾溶液
a酸性KMnO4溶液 b CCl4 c NaOH溶液 d CuSO4溶液
反应① :;
反应③ :;
反应⑦ :。
a.苯和乙炔都能使溴水褪色,前者为化学变化,后者为物理变化
b.苯和乙炔在空气中燃烧都有浓烟产生
c.苯与浓硝酸混合,水浴加热55~60℃,生成硝基苯
d.聚乙炔是一种有导电特性的高分子化合物
![]()
A物质所含官能团的名称是。
a. CH3CH3
b. CH3CHCl2
c. CH3CH2Br
检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2 , 加热,其现象是。

①试管a中生成乙酸乙酯的化学方程式是。
②实验开始时,试管b中的导管不伸入液面下的原因是。
|
①称取E4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. |
①有机物E的相对分子量为:. |
|
②将此9.0gE在足量纯O2充分燃烧,并使其产物依次通过碱石灰、无水硫酸铜粉末、足量石灰水,发现碱石灰增重14.2g,硫酸铜粉末没有变蓝,石灰水中有10.0g白色沉淀生成;向增重的碱石灰中加入足量盐酸后,产生4.48L无色无味气体(标准状况). |
②9.0g有机物E完全燃烧时,经计算:生成CO2共为 mol. |
|
③经红外光谱测定,证实其中含有羟基,羧基,甲基 |
④写出E与NaHCO3溶液反应的化学方程式。