 B .
B .  C .
C .  D .
D . 








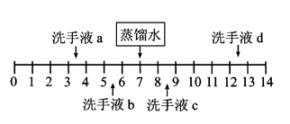
甲:只用水,就有办法鉴别NH4NO3、NaOH、CaCO3和NaCl四种固体;
乙:利用CO2气体就能区分NaOH、Ca(OH)2和稀盐酸三种溶液;
丙:有酚酞和BaCl2溶液,就能鉴别盐酸、硫酸、Na2CO3、NaOH和KNO3五种溶液;
丁:不用其它任何试剂就能将HCl、BaCl2、Na2CO3、NaCl四种溶液鉴别出来。
下列有关这些方案的评价正确的是( )
①若0<b<a,滤液中一定没有Fe(NO3)2
②若b=a,滤液中一定有Mg(NO3)2、Zn(NO3)2和Fe(NO3)2 , 可能有Cu(NO3)2
③若b>a,向滤渣中加稀盐酸,不可能有气泡产生
④若b>a,且忽略过滤操作中溶液损失,滤液中溶质的质量一定<原混合溶液溶质的质量
Ⅰ.取样于烧杯中,加足量水充分溶解,过滤得到白色沉淀物A和滤液;
Ⅱ.往滤液中加入过量的呈中性的氯化钡溶液,发现有白色沉淀B生成。待浊液澄清后,往上层清液中滴加酚酞试液,发现溶液呈无色;
Ⅲ.取白色沉淀B,加入足量稀硝酸,发现有无色气体产生且沉淀全部消失。
请回答下列问题:




【查阅资料】①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是(用化学方程式表示)
②K2CO3溶液呈碱性,CaCl2溶液,KCl溶液呈中性。
【猜想假设】假设I:只含KOH;假设II:含KOH和K2CO3;假设III:只含K2CO3。
【进行实验】
|
实验操作步骤 |
实验现象 |
实验结论 |
|
a.取少量样品于试管中,加入足量的稀盐酸 |
有气泡产生 |
假设 错误 |
|
b.另取少量样品于试管中,加水溶解,加入过量的CaCl2 溶液,振荡,静置 |
产生白色沉淀 |
猜想 II 正确 |
|
c.取②中上层清液,滴加无色的酚酞试液 |
|
【拓展应用】完全变质的 KOH 也有利用价值,从K2CO3的组成或性质看,K2CO3在农业上的用 途是 (填一种即可)。
实验室中用一氧化碳还原纯净的Fe2O3粉末.
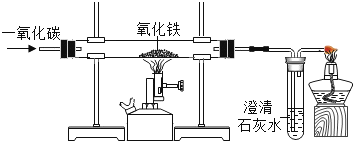
反应后装置中玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小军同学提出了质疑,于是同学们提出查阅资料,寻求真理.
【查阅资料】
①一氧化碳还原Fe2O3的固体产物的成分与反应温度、时间 有关,产物可能是Fe3O4、FeO、Fe
②几种物质的性质
|
物质 性质 |
Fe |
Fe2O3 |
FeO |
Fe3O4 |
|
颜色 |
黑色 |
红色 |
黑色 |
黑色 |
|
能否被磁铁吸引 |
能 |
不能 |
不能 |
能 |
③已知反应:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,FeCl3溶液呈棕黄色
【实验探究】
猜想Ⅰ:全部为Fe
猜想Ⅱ:全部为Fe3O4
猜想Ⅲ: (填化学式)
将黑色粉末加入到足量的稀盐酸中,全部溶解,观察现象:
①有无色气体产生,证明该固体中一定含有 (填化学式).
②溶液呈棕黄色
由上述实验现象,得出上述猜想 正确.
装置中澄清石灰水的作用是 .
若撤出装置中点燃的酒精灯可能造成的后果 .
实验步骤一:取a克上述生铁样品放入一洁净干燥烧杯中,进行如下实验。
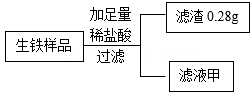
(实验中所得滤渣是用蒸馏水洗涤、干燥后再进行称量。)
实验步骤二:另取a克该生铁样品,进行如图所示实验,实验装置气密性良好。
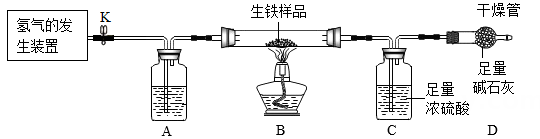
A装置瓶中盛放的试剂是浓硫酸。实验结束后,C装置内浓硫酸的质量增加了0.54克。
实验步骤三:小组同学取实验步骤二中B装置硬质玻璃管内反应后所得全部黑色粉末进行了如下实验,所用装置和滤渣已略去。



[提出问题]碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
[作出猜想]猜想①:CO;猜想②:CO2;猜想③:CO和CO2。
[设计方案]实验装置如图乙。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
方案一:从定性观察角度判断猜想①成立的实验现象是
方案二: 从定量计算角度判断。
取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
|
反应前的质量 |
反应后的质量 |
|
|
A(玻璃管+固体) |
m1 |
m2 |
|
B+C(广口瓶+混合液) |
m3 |
m4 |


一般情况来看, 金属的冶炼与金属的性质有关, 如图是铁、 铜、 铝三种金属冶炼的先后顺序, 则这三种金属的活泼由强到弱是:。


试可答下列问题: