选项 | 陈述I | 陈述II |
A | 金属钠在 | |
B | 碳酸钠受热分解产生 | 用碳酸钠作膨松剂制作面包 |
C | 浓硫酸与 | 可用钢瓶运输浓硫酸 |
D | | 船身焊接锌块可减缓船体腐蚀 |
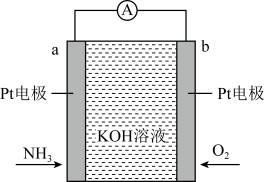
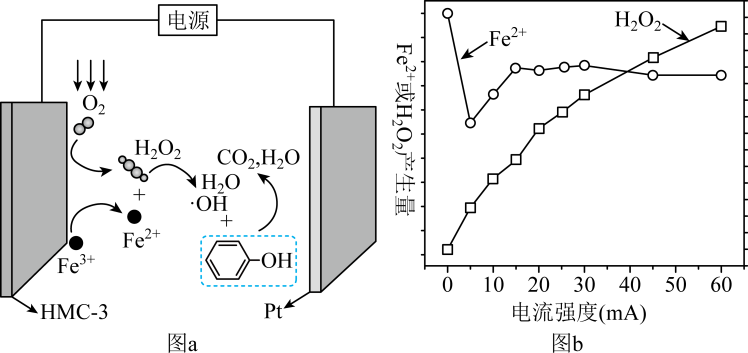
下列说法错误的是( )
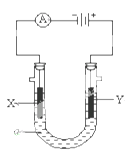
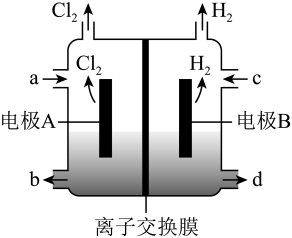
① Y电极上的电极反应式为
② 电解池中X极上的电极反应式为。在X 极附近观察到的现象是。
① X电极的材料是,电极反应式是。
② Y电极的材料是, 电极反应式是。(说明:杂质发生的电极反应不必写出)
kJ/mol
写出与
反应生成
和水蒸气的热化学反应方程式。



序号 | ① | ② | ③ | ④ |
滴入试剂 | AgNO3溶液 | 淀粉KI溶液 | KSCN溶液 | K3[Fe(CN)6]溶液 |
实验现象 | 产生沉淀 | 无蓝色出现 | 无红色出现 | 无蓝色沉淀 |
供选择的实验用品:FeCl2溶液,CuSO4溶液,铜棒,锌棒,铁棒

实验现象:。

我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附CO2生成碳酸锂,该技术设备操作简单,功能可靠,适用于短期出舱任务。吸附发生的化学方程式为。
以固态胺作为吸附剂,吸附CO2与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出CO2 , 从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是变化(填“物理”或“化学”)
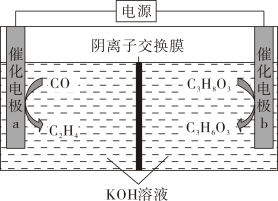
利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如下图所示。
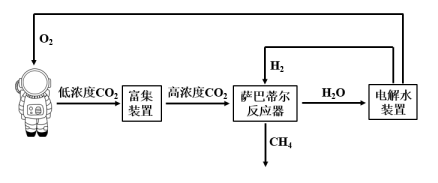
下列说法错误的是____。(双选)
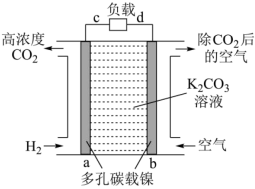
b极为极(填“正”或“负”,),a电极上发生的电极反应。
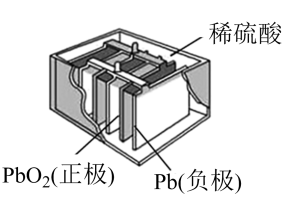
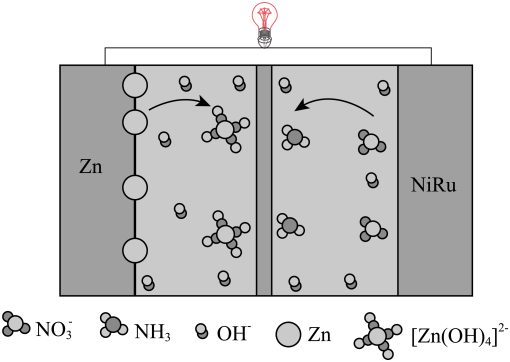
负极;正极。
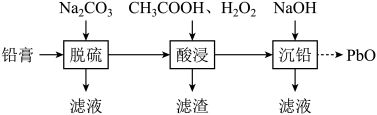
一些难溶电解质的溶度积常数如下表:
难溶电解质 | ||||
一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属氢氧化物 | ||||
开始沉淀的pH | 2.3 | 6.8 | 3.5 | 7.2 |
完全沉淀的pH | 3.2 | 8.3 | 4.6 | 9.1 |
回答下列问题:
在“脱硫”中转化反应的离子方程式为;
饱和溶液中
。
①能被氧化的离子是;
②促进了金属Pb在醋酸中转化为
, 其化学方程式为。
③也能使
转化为
,
的作用是。
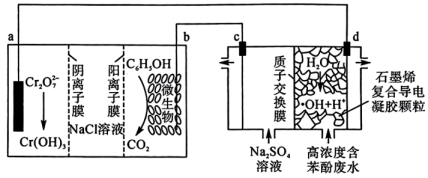
a.主要在阴极室产生
b.在电极上放电,可能产生
c.阳离子交换膜破损导致向阳极室迁移,可能产生
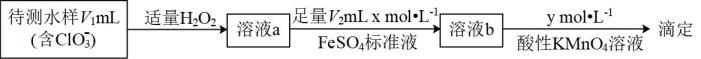
①加入的目的是消耗水样中残留的
和
。若测定中未加入
, 则测得的水样中
的浓度将(填“偏大”“偏小”或“不受影响”)。
②滴定至终点时消耗酸性
溶液,水样中
的计算式为。
①反应的离子方程式为。
②处理时,盐酸可能的作用是:
i.提高 , 使
氧化性提高或
还原性提高;
ii.提高 , 。
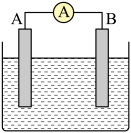
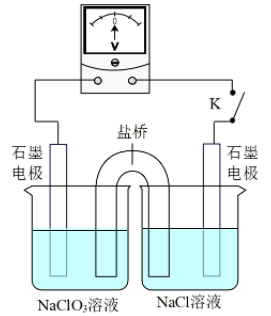
③用如图装置验证i,请补全操作和现象:闭合K,至指针读数稳定后,。
铝片表面除去油垢后,用2mol/LNaOH溶液在60~70℃下洗涤,除去铝表面薄氧化膜,离子方程式为:;再用10%(质量分数)的HNO3溶液对铝片表面进行化学抛光。若取一定体积68%(质量分数)的浓硝酸配制该化学抛光液,需要用到的玻璃仪器有、、玻璃棒和胶头滴管。
取预处理过的铝片和铅做电极,控制电流恒定为0.06A,用直流电源在5~6mol/L硫酸中电解。其中铝片接电源极,产生氧化膜的电极反应式为氧化膜的生长过程可大致分为A、B、C三个阶段(如图所示),C阶段多孔层产生孔隙的离子反应方程式为,A阶段电压逐渐增大的原因是。

取出阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液(3gK2Cr2O7+75mL水+25mL浓硫酸),用秒表测定表面颜色变为绿色(产生Cr3+)所需时间,可判断氧化膜的耐腐蚀性。写出该变色反应的离子方程式:。
①取氧化完毕的铝片,测得表面积为4.0cm2 , 洗净吹干,称得质量为0.7654g;
②将铝片浸于60℃的溶膜液中煮沸10分钟进行溶膜处理;
③取出铝片,洗净吹干,称得除膜后铝片质量为0.7442g。
已知氧化膜的密度为2.7g/cm3 , 可以计算得出氧化膜厚度为μm(1μm=1×10-4cm)。