 B . 滴加液体
B . 滴加液体  D . 稀释浓硫酸
D . 稀释浓硫酸 

①镁和稀硫酸 ②石灰石和稀盐酸 ③氢氧化钠和水 ④碳酸钠和稀硝酸
 向二氧化锰中加入一定量的双氧水
B .
向二氧化锰中加入一定量的双氧水
B .  向一定量的稀盐酸中加入氢氧化钠溶液至过量
C .
向一定量的稀盐酸中加入氢氧化钠溶液至过量
C .  向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D .
向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D .  向等质量的镁粉和铝粉中分别加入过量等质量分数的稀硫酸
向等质量的镁粉和铝粉中分别加入过量等质量分数的稀硫酸


[提出猜想]猜想一:Na2SO4;猜想二:Na2SO4和NaOH;猜想三:Na2SO4、H2SO4。
小刚同学认为猜想一定错误,原因是。
[进行实验]为了验证其它猜想,小刚同学设计了如下实验:
实验操作 | 实验现象 |
取少量反应后溶液于试管中,加入碳酸钠溶液 | 有气泡生成 |
[实验结论]
通过实验,小刚同学认为猜想成立。
[实验反思]根据所学知识,下列哪些物质也能验证该猜想正确?(填序号)。
A.石蕊试液
B.镁
C.氧化铜
D.氢氧化钡

| 实验一 1.用腊粘住的纸片飞落; 2.导购端的小气球鼓起,冷却后又变瘪了; 3.试管上部有冷凝的水珠。 | 实验二 1.染红的水浮在浓硫酸液面上; 2.染红的水受热沸腾,液滴飞溅; 3.可听到像热油锅中滴水的呲呲声; 4.上层的红墨水颜色变黑 |

【设计实验】小组同学经过认真分析思考,提出了自己的假设,并设计了图甲所示的实验A和B进行探究。实验时,观察到试管A中有气泡,试管B中没有气泡,从而验证了自己的假设是成立的。
【迁移应用】一次课外实验的意外现象:镁条放入Na2CO3溶液中,快速产生气泡。
请结合设置对照实验的思想,完成“气体是由什么反应生成的”问题探究。
【实验探究】查阅资料:①镁能与水缓慢反应生成氢气;②Na2CO3溶液呈碱性,其溶液中除了Na+、CO32-、水分子外,还有OH-。
小组同学设计了如图丙对照试验E、F和G。
往镁条中分别加入等量的水、Na2CO3溶液、x溶液进行实验。一段时间后,观察到试管E、G中有气体产生,但缓慢且少,试管F中产生气体既快又多。从对照实验设置的角度分析,实验G所加“x溶液”应该是;
实验一:加热氯酸钾和二氧化锰制取氧气,完全反应后停止加热,得到固体残留物A。
实验二:往铁粉中滴加一定量的稀盐酸,充分反应后,得到混合物B。
实验三:加热铜粉测定空气中的氧气含量,实验结束后得到黑色固体化合物C。





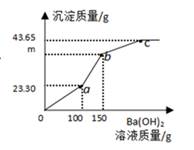
实验一:通过溶液酸碱度证明酸碱发生中和反应,图②中b、c、d三点处对应溶液所含溶质 NaCl的质量大小关系(用b、从、d表示三者关系)。实验二③④⑤操作,(选填“可以”或“不可以”)证明酸与碱发生了中和反应。

①金属表面除锈②实验室制取二氧化碳③除去NaCl中的少量NaOH


|
实验 |
1 |
2 |
3 |
4 |
|
加样品的质量(g) |
5 |
10 |
15 |
20 |
|
生成CO2的质量(g) |
1.76 |
3.52 |
4.4 |
m |
问:

| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
| C瓶溶液增加的质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | 6.6 |
①向少量废液中滴加石蕊试液,试液变红色。
②向10mL废液中滴加Na2CO3溶液,测得沉淀总质量与加入的Na2CO3溶液总质量的关系如表所示,第四次测量:
|
第一次测量 |
第二次测量 |
第三次测量 |
第四次测量 |
|
|
加入Na2CO3溶液的总质量/g |
10 |
20 |
30 |
40 |
|
生成沉淀总质量/g |
a |
0.5 |
1.5 |
1.8 |
请分析计算:
