
取10克生石灰 粉末A质量为12克
气体B
沉淀质量为2.5克
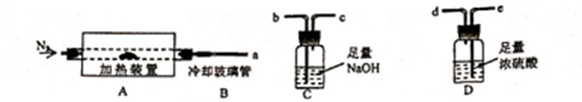
A样品的质量 B装置C的增重
C样品的质量和装置C的增重 D样品分解后残余物的质量
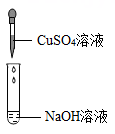
探究1:生成沉淀颜色与反应物的质量比的关系
两种溶液取用的质量及实验现象如表所示(两种溶液混合后充分振荡试管)
|
编号 |
4%的NaOH溶液的质量/g |
8%的CuSO4溶液的质量/g |
沉淀颜色 |
出现黑色物质所等待的时间/min |
|
① |
2 |
2 |
浅绿色 |
不出现 |
|
② |
4 |
待填 |
蓝色中混有浅绿色 |
5 |
|
③ |
6 |
2 |
蓝色 |
3 |
按探究1中③的方法制备5份含蓝色沉淀的混合物,处理方式和实验结果如表所示:
|
编号 |
① |
② |
③ |
④ |
⑤ |
|
处理方式 |
不做处理 |
直接向试管中加8mL水 |
直接向试管中加16mL水 |
滤出蓝色沉淀,洗涤至中性后放入洁净试管,加8mL水 |
滤出蓝色沉淀,洗涤至中性后放入洁净试管,加8mL 4%的Na2SO4溶液 |
|
出现黑色物质所等待的时间/min |
3 |
11 |
17 |
不出现 |
不出现 |
判断④中的蓝色沉淀已洗涤至中性的操作是。
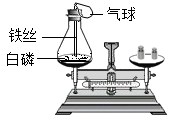
[实验思路]先确认化学反应已经发生,再比较反应物的质量总和和生成物的 质量总和是否相等。
[实验步骤]
I.锥形瓶内装人白磷,塞紧瓶塞放在天平托盘上,调节平衡:
II.取下锥形瓶,将瓶塞上的铁丝在酒精灯上烧红后,接触引燃白磷,并立即塞紧瓶塞;
III.待反应结束冷却后,将锥形瓶放回天平托盘上,观察。
[实验结论]参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
[交流反思]
⑴要确认化学反应已经发生,本实验中观察到的现象是。
⑵反应结束后。若白磷有剩余,你认为是否仍能得出上述结论,并请说明理由。。
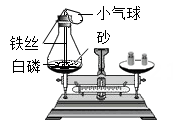
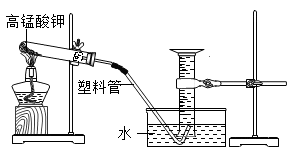
在白磷燃烧前后质量测定实验中(如图)。气球的作用有。
材料二:1703年,施塔尔提出“燃素学说”,其主要观点有:
① 燃素是组成物体的一种成分,一般条件下被禁锢在可燃物中;
②燃素在可燃物燃烧时会分离出来,且燃素可穿透一切物质。
材料三:1756年,罗蒙诺索夫重做了玻义耳的实验。他将金属铅装入容器后密封、称量。然后把容器放到火上加热,白色的金属变成了灰黄色,待容器冷却后再次称量,发现容器的总质量没有发生变化。罗蒙诺索夫对此的解释是:“容器里原来有一定量的空气,且容器中的空气质量减少多少,金属灰的质量就比金属增加多少,在化学变化中物质的质量是守恒的。”后来,拉瓦锡等科学家经过大量的定量实验,推翻了“燃素学说”,质量守恒定律得到公认。

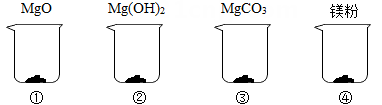
分别取4.2克MgO、Mg(OH)2、MgCO3和“镁粉”置于烧杯中,逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失。四种固体消耗稀盐酸的质量如表所示,且烧杯③和烧杯④中产生了大量气泡。请结合实验现象和数据回答问题。
|
物质 |
MgO |
Mg(OH)2 |
MgCO3 |
“镁粉” |
|
消耗稀盐酸的质量/克 |
121.8 |
m |
58.0 |
61.9 |
|
碳酸钠溶液总质量/g |
25.0 |
50.0 |
75.0 |
100.0 |
125.0 |
150.0 |
175.0 |
200.0 |
|
气体总质量/g |
1.1 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
|
沉淀总质量/g |
0 |
0 |
2.5 |
5.0 |
m |
n |
9.0 |
9.0 |
|
实验次数 |
1 |
2 |
3 |
4 |
5 |
|
加入稀盐酸的质量/克 |
20 |
20 |
20 |
20 |
20 |
|
剩余固体的质量/克 |
8.0 |
6.0 |
4.0 |
2.2 |
2.2 |
回答下列问题:

性质一:2NaHCO3=Na2CO3+CO2↑+H2O,(NaHCO3在50℃以上开始逐渐分解)
性质二:NaHCO+HCl==NaCl+H2O+ CO2↑

|
序号 |
反应前 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
加入稀硫酸溶液质量/克 |
0 |
10 |
10 |
0 |
10 |
10 |
|
C装置中溶液总质量/克 |
100.0 |
101.1 |
102.2 |
103.3 |
104.4 |
105.0 |
(2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑)



|
烧杯1 |
烧杯2 |
烧杯3 |
|
|
样品溶液(克) |
10 |
20 |
30 |
|
氯化钙溶液(克) |
30 |
30 |
30 |
|
沉淀质量(克) |
2 |
4 |
5 |
(Na2CO3+CaCl2=CaCO3↓+2NaCl)
|
实验序号 |
1 |
2 |
3 |
4 |
5 |
|
加入CaCl2溶液质量/克 |
15 |
15 |
15 |
15 |
15 |
|
生成沉淀的总质量/克 |
3 |
m |
9 |
10 |
10 |

求:
取该厂的某钢样粉末28.36g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3g白色沉淀.
|
实验序号 |
Ⅰ |
Ⅱ |
Ⅲ |
|
加入钢样粉末的质量/g |
2.836 |
5.672 |
8.508 |
|
生成气体的体积(标准状况)/L |
1.12 |
2.24 |
2.80 |
请根据表中数据计算硫酸中H2SO4的质量分数.

|
测量次数 |
第1次 |
第6次 |
第16次 |
第21次 |
第26次 |
|
滴加的盐酸总质量/g |
0 |
5 |
15 |
20 |
25 |
|
溶液总质量/g |
50 |
55 |
m |
69.78 |
74.78 |
|
溶液pH |
12.4 |
12.1 |
7.0 |
2.2 |
2.1 |
请分析计算:

①取200g混合溶液加入足量的AgNO3溶液,经过滤洗涤、干燥、称量得到143.5gAgCl固体;
②另取原混合溶液各200与含有杂质的废铁用反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
|
实验组别 |
一 |
二 |
三 |
四 |
五 |
|
混合溶液质量/g |
200 |
200 |
200 |
200 |
200 |
|
铁屑质量/g |
6 |
9 |
12 |
15 |
18 |
|
析出铜的质量/g |
6.4 |
9.6 |
m |
16 |
16 |
请分析计算:

|
实验次数 |
1 |
2 |
3 |
|
碳酸钠质量/克 |
0.53 |
1.06 |
2.12 |
|
反应前装置总质量/克 |
66.33 |
66.86 |
67.92 |
|
反应后装置总质量/克 |
66.19 |
66.62 |
67.42 |
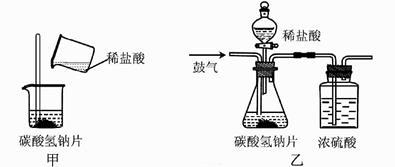
实验序号 | 1 | 2 | 3 |
碳酸氢钠片样品质量/克 | 3.0 | 3.0 | 3.0 |
反应前总质量/克 | 193.8 | 194.6 | 193.6 |
反应后总质量/克 | 192.6 | 193.6 | 192.5 |
二氧化碳质量/克 |
|
|
|
请计算药片中碳酸氢钠的质量分数。