实验 | 现象 | 结论 | |
A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |

选项 | 物质 | 性质用途 |
A | 电子跃迁到激发态过程中释放能量,产生紫色光 | 钾盐用作紫色烟花原料 |
B |
| 葡萄酒中添加 |
C | 高铁酸钾具有强氧化性 | 可用作饮用水的消毒剂 |
D |
| 环保工程师用熟石灰处理酸性废水 |
实验操作 | 现象 | 结论 | |
A | 向Ba(OH)2溶液中滴加少量稀硫酸 | 电导率减小 | 溶液中的离子浓度减小 |
B | 向盛有SO2水溶液的试管中滴加几滴酸性KMnO4溶液,振荡 | 酸性KMnO4溶液褪色 | SO2具有漂白性 |
C | 向乙醇中加入一小粒金属钠 | 有气体产生 | 乙醇中含有水 |
D | CH4和Cl2按1:1混合,光照 | 试管壁出现油状液滴 | 油状液滴为CH3Cl |

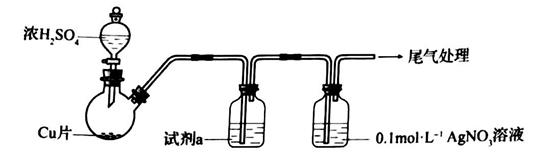
①浓 与Cu反应的化学方程式是
②试剂a是。
(资料: 微溶于水;
难溶于水)
实验二:验证B的成分

①写出 溶于氨水的离子方程式:。
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是 ,进而推断B中含有
。向滤液E中加入一种试剂,可进一步证实B中含有
。所用试剂及现象是。
途径1:实验一中, 在
溶液中被氧化生成
,随沉淀B进入D。
途径2:实验二中, 被氧化为
进入D。
实验三:探究 的产生途径
①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有;取上层清液继续滴加 溶液,未出现白色沉淀,可判断B中不含
。做出判断的理由:。
②实验三的结论:。
根据上述实验所得结论:。
从图1中选择符合图2要求的X代表的物质:X。



装置乙的作用是。若X为品红溶液,观察到溶液褪色,说明SO2具有(填序号,下同);若X为Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有。
a.氧化性 b.还原性 c.漂白性 d.酸性
Ca2++ClO-+SO2+H2O=CaSO4↓+Cl-++H+