
选项 | 生产活动 | 化学原理 |
A | 乙烯水化法制工业酒精 | 乙烯可发生加成反应 |
B | 利用明矾净水 | Al3+有氧化性 |
C | 利用硅做太阳能电池 | 硅是半导体材料 |
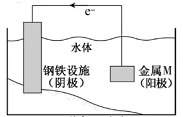
D | 轮船铁护栏上绑一块锌 | 牺牲阳极保护阴极 |
①氯化铁溶液具有酸性,可用作刻蚀铜电路板
②二氧化氯具有强氧化性,可用作饮用水消毒
③氧化钙具有很强的吸水性,可用作食品干燥剂
④石英坩埚耐高温,可用来加热熔化烧碱纯碱等固体
⑤活性炭具有极强的吸附能力,可用作制糖业的脱色剂
⑥铜的金属活泼性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀

| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 氯乙烷加入NaOH溶液加热,冷却后加入AgNO3溶液 | 产生沉淀 | 证明氯乙烷已经水解 |
| B | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴加几滴K3[Fe(CN)6]溶液 | 无明显现象 | 锌对铁依然具有保护作用 |
| C | 向氯化钠粉末中加入适量酒精充分震荡形成无色透明液体,用红色激光笔照射 | 出现一条光亮的通路 | 形成的分散系是胶体 |
| D | 向某钠盐溶液中加入盐酸,将产生的气体通入硝酸酸化的BaCl2溶液中 | 有白色沉淀产生 | 反应生成的气体可能是SO2 |
| 实验 | 0~1h | 1h | 2h | |
| 1 | 6mol/L盐酸 | 无气泡产生 | ||
| 2 | 3mol/L硫酸 | 无气泡产生 | 黄铜表面出现少量小气泡,反应缓慢 | 黄铜表面小气泡数量增加不明显,反应缓慢 |
| 3 | 6mol/L硝酸 | 2min时出现较多气泡,反应迅速进行;10min时出现明显的红棕色气体 | 溶液变为蓝色,反应持续进行,但不剧烈 | 溶液变为蓝色,反应持续进行,较为缓慢 |
| 4 | 2mol/L硝酸 | 黄铜表面出现少量小气泡,反应缓慢 | 溶液出现淡蓝色,反应缓慢 | 溶液出现淡蓝色,反应缓慢 |
| 4 | 浓硝酸 | 反应物接触后迅速反应,反应剧烈,产生大量红棕色气体,溶液变为深蓝色 | ||
依据上述实验,所得结论错误的是( )
| ① | ② | ③ |
| | | |
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法错误的是( )
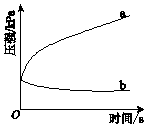
 B . 图乙是平衡体系2NO2(g)
B . 图乙是平衡体系2NO2(g) 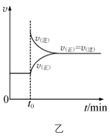 C . 图丙是某温度下c(CH3COOH)+c(CH3COO-)=0.100 mol·L-1的醋酸与醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH的关系,可推知该温度下pH=3的溶液中:Ka<10-4.75
C . 图丙是某温度下c(CH3COOH)+c(CH3COO-)=0.100 mol·L-1的醋酸与醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH的关系,可推知该温度下pH=3的溶液中:Ka<10-4.75  D . 图丁中虚线是2SO2+O2
D . 图丁中虚线是2SO2+O2 

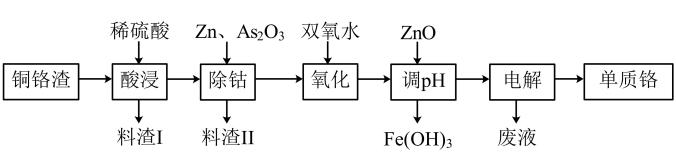
①酸浸时形成的金属离子的价态均相同。加入双氧水时铁、铬形成的离子均被氧化,写出氧化铬形成
的离子方程式为。
②“电解”时,阴极的电极反应式为:。
③三价铬离子能形成多种配位化合物。中提供电子对形成配位键的原子分别是(填元素符号),中心离子的配位数为。
④304不锈钢是生活中常见的一种不锈钢,业内也叫做不锈钢,指必须含有
以上的铬,
以上的镍的不锈钢。铬和镍能形成多种配合物,如
为正四面体构型、
、为正方形构型、
、
为正八面体构型等,下列有关说法正确的是(填选项字母)。
A.中含有共价键和离子键
B.304不锈钢不可长时间盛放盐、酱油、醋、菜汤等,不能用304不锈钢锅煲中药
C.不锈钢不会生锈,哪怕在潮湿恶劣的环境
D.和
中,镍原子均为
杂化

(注:SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃)