
 说法正确的是( )
说法正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 向含有酚酞的 | 出现白色沉淀且溶液红色变浅 |
|
B | 向乙醇中加入绿豆大小的钠块 | 有气泡产生 | 乙醇中含有水 |
C | 用锌与稀硫酸反应制氢气时,滴入几滴硫酸铜溶液 | 反应速率加快 |
|
D | 向 | 得到澄清溶液 |
|
操作 | 现象 | 结论 | |
A | 将缠绕的铜丝灼烧后反复插入盛乙醇的试管,然后滴加酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | 乙醇催化氧化生成乙醛 |
B | 向小苏打粉末中滴入柠檬酸 | 产生无色气体 | 柠檬酸的酸性比碳酸强 |
C | 将25℃、0.1mol·L-1Na2SO3溶液加热到40℃,用传感器监测溶液pH的变化 | 溶液pH逐渐减小 | 温度升高,Na2SO3水解平衡正向移动 |
D | 将苯、液溴、铁粉混合后产生的气体通入AgNO3溶液中 | 产生淡黄色沉淀 | 苯与液溴发生了取代反应 |
 )具有抗菌、抗炎、镇静等作用。下列关于七叶内酯的说法错误的是( )
)具有抗菌、抗炎、镇静等作用。下列关于七叶内酯的说法错误的是( )


| 选项 | 棉花球上蘸的液体 | 固体 | 实验 |
| A | 乙醇 | 氧化铜 | 制备少量乙醛 |
| B | 石蜡油 | 碎瓷片 | 石蜡油的分解 |
| C | 浓氨水 | 无水氯化钙 | 制备干燥的氨气 |
| D | 水 | 铁粉 | 铁粉还原水蒸气 |

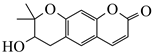 可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合物,下列叙述错误的是( )
可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合物,下列叙述错误的是( )

| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将乙醇与浓硫酸的混合溶液加热,产生的气体直接通入酸性 | 溶液紫色褪去 | 产生的气体一定是乙烯 |
| B | 向 | 得到澄清溶液 | |
| C | 常温下,向含等浓度 | 先生成蓝色沉淀 | 常温下, |
| D | 将用稀硫酸酸化后的 | 溶液变黄 | 氧化性: |
 +HBr
+HBr
 +H2O
+H2O

下列有关说法错误的是
I.环己烯的制备
如图所示,将环己醇加入试管中,再加入
固体,缓慢加热,在试管
内收集到环己烯粗品。

|
|
密度 |
熔点(℃) |
沸点(℃) |
溶解性 |
|
环己醇 |
0.96 |
25 |
161 |
能溶于水 |
|
环己烯 |
0.81 |
|
83 |
难溶于水 |
向环己烯样品中加入
, 充分反应后,剩余的
与足量
溶液反应,用
标准溶液滴定,终点时消耗
。 (已知:
)
滴定所用指示剂为,滴定终点现象为。
①能与溶液发生显色反应;
②最多消耗
;
③核磁共振氢谱中有4组峰,其峰面积之比为;
 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。
①谱和IR谱检测表明:分子中共有6种不同化学环境的氢原子,有N-H键。②分子中仅含一个杂原子的六元环,环上只有一条侧链。

已知:反应时强烈放热;过量氧化剂会将环己醇氧化为己二酸。
| 物质 | 相对分子质量 | 沸点/℃ | 密度/(g∙cm-3 , 20℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
实验步骤:
I.配制氧化液:将5.5g重铬酸钠配成溶液,再与适量浓硫酸混合,得橙红色溶液,冷却备用。
II.氧化环己醇:向盛有5.3mL环己醇的反应器中分批滴加氧化液,控制反应温度在55~60℃,
搅拌20min。
III.产物分离:向反应器中加入一定量水和几粒沸石,改为蒸馏装置,馏出液为环己酮和水的混合液。
IV.产品提纯:馏出液中加入NaCl至饱和,分液,水相用乙醚萃取,萃取液并入有机相后加入无水MgSO4干燥,水浴蒸除乙醚,改用空气冷凝管蒸馏,收集到151~156℃的馏分2.5g。
回答下列问题:

①反应器的名称是;控制反应温度在55~60℃的措施除分批滴加氧化液外,还应采取的方法是。
②温度计示数开始下降表明反应基本完成,此时若反应混合物呈橙红色,需加入少量草酸,目的是 。

已知:
① ![]() +
+ ![]()
 (其中一种产物)
(其中一种产物)
② ![]() +
+ ![]()
![]() +R2OH
+R2OH
③烯醇式( ![]() )结构不稳定,容易结构互变,但当有共轭体系(苯环、碳碳双键、碳氧双键等)与其相连时变得较为稳定。
)结构不稳定,容易结构互变,但当有共轭体系(苯环、碳碳双键、碳氧双键等)与其相连时变得较为稳定。
①属于芳香族化合物,但不含甲基;
②与FeCl3溶液发生显色反应;
③1mol该有机物能与2molNaOH恰好完全反应;
④核磁共振氢谱有4组峰,且峰面积之比为2:2:1:1。
a.遇 溶液显紫色 b.能发生银镜反应 c.能与
发生加成反应
其中核磁共振氢谱显示有5种不同化学环境的氢,峰面积比为1∶2∶2∶1∶2的有机物的结构简式为。