











X | Y | ||
Z | W | Q |
W | X | Y |
Z |
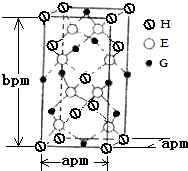
M与Y形成的一种化合物的立方晶胞如图所示.
①该化合物的化学式为,已知晶胞参数a=0.542nm,此晶体的密度为g•cm﹣3 . (写出计算式,不要求计算结果.阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是.此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为.

①H3O+中心原子的杂化类型为,NH4+的空间构型为。
②3[H3ON5]·3[NH4N5]·NH4Cl中阴离子N5-中的 键总数为个。分子中的大
键可用符号
表示,其中m代表参与形成大键的原子数,n代表参与形成大键的电子数(如苯分子中的大
键可表示为
),则N5-中的大
键应表示为。
③图(b)中虚线代表氢键,其中表示式为(NH4)N一H……Cl、、。
A | 原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
B | 基态原子的p轨道电子数比s轨道电子数少1 |
C | 位于第2周期,原子核外有3对成对电子、两个未成对电子 |
d | 位于周期表中第7纵列 |
e | 基态原子M层全充满,N层只有一个电子 |
请回答:

①基态Ti3+的电子排布式为;LiBH4中Li、B、H 元素的电负性由大到小的排列顺序为。
②另有一种含钛元素的新型材料,其理论结构模型如图所示,图中虚线框内碳原子的杂化轨道类型为。

①NH3BH3中是否存在配位键(填“是”或“否”);与NH3BH3互为等电子体的分子的化学式为。
②B、C、N 与O元素的第一电离能由大到小的顺序为。
③氨硼烷在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则立方氮化硼晶体可用作(选填下列字母序号)。
a.切削工具
b.钻探钻头
c.导电材料
d.耐磨材料
①若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式为;
②铜与其它许多金属及其化合物都可以发生焰色反应,其原因是。
I1/KJ·mol-1 | I2/KJ·mol-1 | I3/KJ·mol-1 | I4/KJ·mol-1 | I5/KJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
①该金属元素是(填元素符号)..
②若氢化物的晶胞结构如图所示(有4 个H原子位于面上,其余H原子位于晶胞内),已知该晶体的密度为ρg·cm-3 , 则该晶胞的体积为cm3[用含ρ、NA的代数式表示(其中NA为阿伏加德罗常数的值)]。


②X、Z、W最高价氧化物水化物酸性由强到弱依次是。(填化学式)。
②含Y元素的盐与小苏打溶液可用作泡沫灭火剂,写出灭火时发生反应的离子方程式。

请回答下列问题:
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
工业上用电解法制G的单质的化学方程式是,若以石墨为电极,阳极产生的混合气体的成分是(写化学式).
CO的结构可表示为CO,元素Y的单质Y2的结构也可表示为YY.如表是两者的键能数据(单位:kJ•mol﹣1):
A﹣B | A═B | A≡B | |
CO | 357.7 | 798.9 | 1071.9 |
Y2 | 154.8 | 418.4 | 941.7 |
①结合数据说明CO比Y2活泼的原因:.
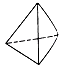
②意大利罗马大学Fulvio Cacace等人获得了极具研究意义的Y4分子,其结构如图所示,请结合上表数据分析,下列说法中,正确的是.
A.Y4为一种新型化合物
B.Y4与Y2互为同素异形体
C.Y4的沸点比P4(白磷)高
D.1mol Y4气体转变为Y2将放出954.6kJ热量.

其中碳原子的杂化方式为,个数比为.
钨元素位于周期表的第六周期第VIB族,请写出其外围电子排布式,
A.Fe CuB.Ti AuC.Mg ZnD.Cu Ag