 B .
B . 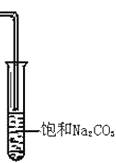 C .
C .  D .
D . 
A | B | C | D |
|
|
|
|
混合反应物 | 生成乙酸乙酯 | 收集乙酸乙酯 | 分离出乙酸乙酯 |
 B .
B .  C .
C .  D .
D . 

实验目的 | 实验操作 | |
A | 检验溶液中的Fe2+ | 先滴加新制氯水,再滴加KSCN溶液 |
B | 配制0.5mol/L的H2SO4溶液 | 量取50mL1.0 mol/L H2SO4溶液,倒入小烧杯中,再加入50mL水稀释 |
C | 验证乙烯的生成 | 加热乙醇和浓硫酸混合液,将气体通入酸性KMnO4溶液 |
D | 除去乙酸乙酯中混有的乙酸 | 用过量饱和碳酸钠溶液洗涤后分液 |


|
|
|
|
A.混合乙醇和浓硫酸 | B.制取乙酸乙酯 | C.分离乙酸乙酯和水层 | D.除去乙酸乙酯中的杂质 |
| 实验目的 | 玻璃仪器 | 试剂 | |
| A | 配制100mL一定物质的量浓度的NaCl溶液 | 100mL容量瓶、胶头滴管、烧杯、量筒、玻璃棒 | 蒸馏水、NaCl固体 |
| B | 制备Fe(OH)3胶体 | 烧杯、酒精灯、胶头滴管 | 蒸馏水、饱和FeCl3溶液 |
| C | 测定NaOH溶液浓度 | 烧杯、锥形瓶、胶头滴管、酸式滴定管 | 待测NaOH溶液、已知浓度的盐酸、甲基橙试剂 |
| D | 制备乙酸乙酯 | 试管、量筒、导管、酒精灯 | 冰醋酸、无水乙醇、饱和Na2CO3溶液 |



已知:A中放有浓硫酸;B中放有乙醇、无水碳酸钠;D中放有饱和碳酸钠溶液.
有关有机物的沸点.
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
则试剂a是:,试剂b是:.分离方法I是,分离方法II是
试解答下列问题:
①甲实验失败的原因是:.
②乙实验失败的原因是:.
①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;
②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;
③小火加热a试管中的混合液;
④等b试管中收集到约2mL产物时停止加热.撤下b试管并用力振荡,然后静置待其中液体分层;
⑤分离出纯净的乙酸乙酯.

请回答下列问题:
实验编号 | 试管a中试剂 | 试管b中试剂 | 测得有机层的厚度/cm |
A | 3mL乙醇、2mL乙酸、1mL18mol•L﹣1 浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
B | 3mL乙醇、2mL乙酸 | 0.1 | |
C | 3mL乙醇、2mL乙酸、6mL 3mol•L﹣1 H2SO4 | 1.2 | |
D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.实验D中应加入盐酸的体积和浓度分别是 mL和 mol•L﹣1 .
②分析实验(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.浓硫酸的吸水性能够提高乙酸乙酯产率的原因是.
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是.
④分离出乙酸乙酯层后,经过洗涤杂质;为了干燥乙酸乙酯可选用的干燥剂为(填字母).
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体
⑤为充分利用反应物,该同学又设计了图2中甲、乙两个装置(利用乙装置时,待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).你认为更合理的是.理由是:.

①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管中加入1mL2%的AgNO3溶液.
实验装置如下图所示:

试管①中反应的化学方程式为。
反应结束后在试管②中看到分层现象,上层为无色透明的油状液体。取下试管②进行振荡,下层溶液红色褪去。甲同学认为下层溶液褪色是蒸出的乙酸中和了碳酸钠,乙同学通过查阅资料对甲同学的推测产生质疑。
资料:酚酞是一种白色晶状粉末,不溶于水,可溶于乙醇。酚酞试剂是酚酞的乙醇溶液。
乙同学的推测是:。
实验1:
甲同学用pH计测得饱和碳酸钠溶液(浓度约为2mol/L)的pH为12.23;
按照上述方法进行乙酸乙酯的制取实验,实验结束后,取振荡后的试管②中下层无色液体,分成三份,分别完成以下实验:
|
序号 |
实验操作 |
实验现象 |
实验结论 |
|
a |
滴加几滴酚酞试剂 |
溶液变红 |
|
|
b |
滴入乙酸溶液 |
|
|
|
c |
用pH计测溶液pH |
pH为12.21 |
b中现象为,实验1的结论。
|
序号 |
操作 |
现象 |
|
d |
试管②中分离出的上层液体,加入饱和碳酸钠溶液,振荡 |
溶液变成浅红色,静置分层后红色消失 |
|
e |
取5mL饱和碳酸钠溶液,滴入几滴酚酞试剂,再加入与试管②中上层液体体积相等的纯净的乙酸乙酯,振荡 |
|
e中的实验现象为。
III.拓展延伸
在以上实验过程中,丙同学还有新的发现,他查阅到以下资料:
资料:室温下,当酚酞试剂滴入pH>13的无色溶液时,溶液先变红,静置后褪色。
据此资料,丙同学想到了一种区分1mol/L碳酸钠溶液和1mol/L氢氧化钠溶液的方法,这种方法是。

①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
A.加入2mL浓硫酸 B.加入3mL乙醇 C.加入2mL乙酸
Ⅰ.乙酸乙酯粗产品的制备(如图所示省略夹持仪器和加热装置)

Ⅱ.乙酸乙酯纯化的流程

回答下列问题:
编号 | 三颈烧瓶中试剂 | 丙中试剂 | 丙中有机层的厚度/cm |
A | 10 mL乙醇、8mL乙酸、5 mL 18mol∙L-1浓硫酸 | 5 mL饱和 溶液 | 2.0 |
B | 10 mL乙醇、8 mL乙酸、5 mLH2O | 0.1 | |
C | 10 mL乙醇、8 mL乙酸、5 mL 2mol∙L-1硫酸溶液 | 0.6 | |
D | 10 mL乙醇、8 mL乙酸、盐酸 | 0.6 |
①为证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积mL,浓度mol∙L-1。
②分析实验A与(填编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。
①在试管甲(如图)中加入一定量浓硫酸、13.8 g乙醇(C2H518OH)和10 mL(密度为1.05 g/cm3)冰醋酸的混合溶液。

②按图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
①浓硫酸②乙醇③冰醋酸

|
物质 |
熔点(℃) |
沸点(℃) |
密度( |
|
乙醇 |
-117.3 |
78.5 |
0.789 |
|
乙酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.90 |
|
浓硫酸(98%) |
338.0 |
1.84 |
制取时的主要步骤为:
①在30mL的大试管A中按体积比1∶4∶4配制浓硫酸、乙醇和乙酸的混合溶液;
②按图连接装置(装置气密性良好),用小火均匀加热装有混合液的大试管3-5min;
③待试管B收集到一定量产物后停止加热;
④分离出乙酸乙酯,洗涤、干燥。
请根据题目要求回答下列问题:

装置中所用冷凝管的全称是。实验时常采用油浴加热,控制反应混合物温度在120℃~125℃。反应温度不是控制在乙酸乙酯沸点附近的主要目的是。该情况下锥形瓶中得到的液体含有的有机物除乙酸乙酯外,还有。
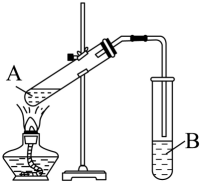
已知:①氯化钙可与乙醇形成CaCl2·6C2H5OH。
②相关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
③2CH3CH2OH CH3CH2OCH2CH3+H2O
装置如图所示,A中盛有浓硫酸,B中盛有9.5 mL无水乙醇和6 mL冰醋酸,D中盛有饱和碳酸钠溶液。

写出乙酸与乙醇发生酯化反应的化学方程式。
①将D中混合液进行分液。
②有机层先用5 mL饱和食盐水洗涤,再用5 mL饱和氯化钙溶液洗涤,最后用水洗涤。然后将有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物。
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯。
第①步分液时,用到的玻璃仪器为烧杯和。


①在该制备反应中浓硫酸的作用是。
②饱和溶液的作用除了吸收B和D,还有。
③丙烯酸乙酯天然存在于波萝等水果中,可以在相同条件下由丙烯酸(CH2=CH-COOH)和B制得,该反应的化学方程式为,其反应类型为。





Ⅰ.反应④的化学方程式是。
Ⅱ.b试管中盛放的饱和碳酸钠溶液作用是;。(任意写两条)
Ⅲ.分离出试管中油状液体用到的主要仪器是。

回答下列问题: