
 D .
D . 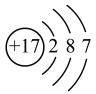 B . H2O的空间填充模型为
B . H2O的空间填充模型为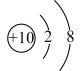 C . 次氯酸钠(NaClO)中Cl元素的化合价:+1
D . NaClO的电离方程式:NaClO=Na++Cl++O2-
C . 次氯酸钠(NaClO)中Cl元素的化合价:+1
D . NaClO的电离方程式:NaClO=Na++Cl++O2-

 C . 基态
C . 基态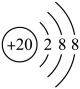 C . CH4的球棍模型:
C . CH4的球棍模型: 
已知: 。
。
回答下列问题:
A的化学名称为。
有机物F是布洛芬的同系物,F的同分异构体同时满足下列条件的总数为种。

a.相对分子质量比布洛芬小28;
b.苯环上仅有两个取代基,且羧基与苯环直接相连。
其中分子中核磁共振氢谱有4组吸收峰,峰值比为9:2:2:1,布洛芬的结构简式为。

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有、
。
②“酸浸”时,锑元素反应生成难溶的浸渣。
回答下列问题:
A. B.
C.
D.
②“氯盐酸浸”时,通入的目的是。
