




物质性质 | 实际应用 | |
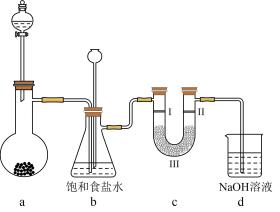
A | 硅为半导体材料 | SiO2用于光纤通讯 |
B | Cl2具有氧化性 | 氯水可以漂白有色布条 |
C | Al表面易形成致密的氧化物薄膜 | 可以用铝槽车运送热的浓硫酸 |
D | 乙醇可以使蛋白质变性 | 乙醇用于制作医用酒精 |
|
选项 |
性质 |
用途 |
|
A |
CCl4难溶于水,难于燃烧 |
CCl4常用作有机溶剂和灭火剂 |
|
B |
Al2O3既能与强酸反应,又能与强碱反应 |
Al2O3常用作耐高温材料 |
|
C |
SiO2透明,折射率合适,能够发生全反射 |
SiO2用作光导纤维材料 |
|
D |
Cl2具有漂白性 |
常用Cl2对自来水进行杀菌消毒 |
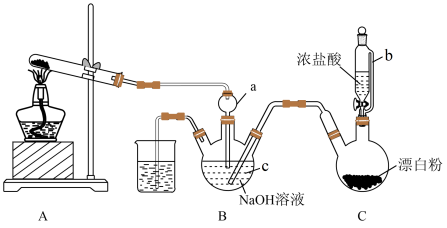
 B . 净化Cl2
B . 净化Cl2 C . 收集Cl2
C . 收集Cl2 D . 尾气处理
D . 尾气处理
漂白液的有效成分为NaClO, NaClO在40℃以上容易分解,可通过Cl2与冷的NaOH溶液反应制得。
制备装置如图所示。

该实验中不能替代KClO3的药品是。
a.MnO2 b.K2Cr2O7 c.KMnO4 d.Ca(ClO)2
已知: Ka1(H2CO3)=4.2 ×10-7 , Ka2(H2CO3)=5.6 ×10-11;
Ka1(H3PO4 )=7.6 ×10-3 , Ka2(H3PO4)=6.3 ×10-8 , Ka3(H3PO4)=4.4 ×10-13。
若最终氯钠的化学式中a=3,b=1则该步骤中所用NaOH与H3PO4的物质的量之比为,
将Ⅰ与Ⅱ制得的溶液常温下充分混合搅拌,减压蒸发,低温干燥,得氯钠晶体。
减压蒸发的目的是。
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
离子 | Na+ | K+ | NH | H+ | SO | NO | Cl- |
浓度/(mol·L-1) | 6×10-6 | 4×10-6 | 2×10-5 | a | 4×10-5 | 2×10-5 | 3×10-5 |
根据表中数据计算,检测的溶液pH=。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体L(标准状态)。

ⅱ.随着反应进行,……
[进行实验]将反应后的固液混合物倒出,平均分在2个试管中,分别进行以下实验,证实了猜想ⅰ不成立。
|
序号 |
实验操作 |
实验现象 |
|
Ⅰ |
将湿润的淀粉碘化钾试纸放置于试管口,加热试管;,充分振荡,继续加热 |
试纸未变蓝 |
|
Ⅱ |
将湿润的淀粉碘化钾试纸放置于试管口,加热试管;滴入2滴浓硫酸,充分振荡,继续加热 |
滴入浓硫酸前,试纸不变蓝;滴入浓硫酸后,试纸变蓝 |
将Ⅰ中操作补充完整:
序号 | 实验装置 | 实验操作 | 现象 |
Ⅲ |
| 向左侧烧杯中滴加2滴浓硫酸 | 滴加浓硫酸前,电流表指针不偏转;滴加浓硫酸后,电流表指针偏转 |
Ⅳ | 向右侧烧杯中滴加2滴浓硫酸 | 电流表指针始终不偏转 |
滴加浓硫酸后,左边烧杯中反应的电极反应式是。
序号 | 实验操作 | 实验现象 |
Ⅴ | 在0.5g二氧化锰中加入2毫升5%双氧水 | 产生气泡 |
Ⅵ | 在0.5g二氧化锰中滴加2滴浓硫酸,再加入2毫升5%双氧水 | 产生气泡,黑色固体消失,生成无色溶液 |
Ⅵ中反应的离子方程式是。

资料表明:室温下,为无色液体,易挥发,高温时能与
反应,与HCl不发生反应。其他相关信息如下表所示:
物质 | 熔点/℃ | 沸点/℃ | 水溶性 |
-25 | 136.4 | 易水解成白色沉淀,能溶于有机溶剂 | |
-23 | 76.8 | 难溶于水 |
请回答下列问题:

①在滴定管中装入标准溶液的前一步应进行的操作为。
②已知常温下, ,
,
, (
呈砖红色,溴化银呈浅黄色),应选择的指示剂是。
A.KCl B. C.KBr
③根据上述数据计算该产品的纯度为%。

下列有关说法正确的是(填序号)。
a.选择图甲装置的优点是避免过滤过程中析出晶体
b.分离过程为:趁热过滤,蒸发结晶,抽滤,洗涤,干燥
c.选择图乙装置的优点是抽滤速率快,使产品更加干燥
判断达到滴定终点的现象为。产品质量分数为(用含a , c , V的代数式表示)。

①Sn为50号元素,请写出Sn在元素周期表的位置;
②在上述流程中,加入锡粉的作用为;
③反应Ⅰ的离子方程式为;
④操作Ⅰ为沉淀的洗涤,请简述如何判断沉淀已洗涤干净?;操作Ⅱ中,实验操作包括、过滤、洗涤、干燥等一系列操作。

①SnCl4是分子(填“极性”或“非极性”)。
②装置Ⅲ中盛装药品Sn的仪器名称是;装置Ⅵ中碱石灰的作用为。
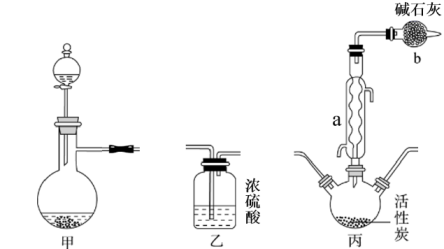
A.98%浓硫酸+Cu B.70%H2SO4+Na2SO3固体
C.浓HNO3+Na2SO3固体 D.70%H2SO4+Na2SO3浓溶液
②甲装置中制备Cl2的化学方程式是。

试回答:
发生装置选择(填“图甲”、“图乙”或“图丙”)。
②装置Ⅰ能防止多余气体逸散的原因是。
③欲用装置Ⅱ(或装置Ⅲ)代替装置Ⅰ中的b~c部分(试剂相同),装置Ⅱ(填“是”或“否”)可行,理由是。装置Ⅲ(填“是”或“否”)可行,理由是。

图中:①的试管里盛有15 mL 30% KOH溶液,置于水浴中;②的试管里盛有15 mL 8% NaOH溶液,置于冰水浴中;③的试管里加有紫色石蕊试液;④为尾气吸收装置。
比较制取氯酸钾和次氯酸钠的条件,二者的差异是①;②。
