选项 | 粒子组 | 判断和分析 |
A | 透明溶液中:Mg2+、Cu2+、Br-、 | 不能大量共存,因为Cu2+呈蓝色 |
B | 能溶解Al2O3的溶液中:Na+ 、 | 能大量共存,粒子间不反应 |
C | NaCl溶液中:Fe3+、I-、Ba2+、CH3COO- | 不能大量共存,Fe3+和I- 会发生氧化还原反应 |
D | NaHSO4溶液中:K+ 、Cl-、 | 不能大量共存, |
选项 | 粒子组 | 判断和分析 |
A |
| 不能大量共存,因发生反应: |
B |
| 不能大量共存, |
C |
| 能大量共存,钠盐、铵盐都溶于水 |
D |
| 不能大量共存, |

选项 | 粒子组 | 判断和分析 |
A |
| 不能大量共存,因发生反应: |
B |
| 不能大量共存,因 |
C |
| 不能大量共存,因 |
D |
| 不能大量共存,因发生反应: |

|
|
操作 |
现象 |
解释或结论 |
|
A |
向滴有酚酞的Na2CO3溶液中加入少量BaCl2固体 |
生成白色沉淀、溶液红色变浅 |
|
|
B |
将0.1 mol•L-1氨水稀释到0.01 mol•L-1 , 用pH计测量其pH |
pH由11.1变为10.6 |
稀释氨水NH3•H2O的电离程度减小 |
|
C |
冰水浴环境下向滴有酚酞的饱和氨盐水中通入过量CO2 |
溶液红色褪去时析出沉淀 |
利用物质溶解度的不同制备NaHCO3 |
|
D |
向2 mL0.1 mol•L-1ZnSO4溶液中加入1 mL1 mol•L-1Na2S溶液,再加入2 mL0.1 mol•L-1CuSO4溶液 |
先出现白色沉淀,后变为黑色沉淀 |
CuS的溶度积比ZnS小 |
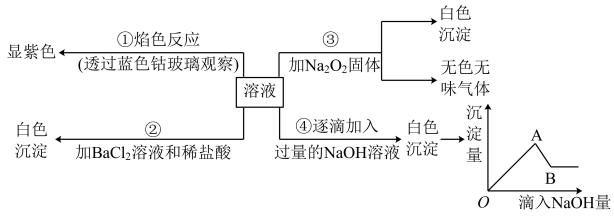
回答下列问题:
阳离子 |
|
阴离子 |
|
为确定它们的组成,进行以下实验:
①分别将它们溶于水,均为无色溶液。
②将A溶液分别滴入其它三种溶液中,均有沉淀生成,继续滴加至过量,B中沉淀逐渐溶解。
③向D溶液中逐滴加入C溶液,先无气体产生,继续滴加产生无色无味气体。
回答下列问题:
⑴用洁净的铂丝蘸取少量溶液进行焰色反应,透过蓝色钴玻璃观察,火焰呈紫色。
⑵取少量原溶液,滴加足量 溶液,有白色沉淀产生,再滴加足量的稀硝酸,无气泡产生且沉淀不溶解,过滤得到滤液a。
⑶另取少量原溶液,逐滴滴加过量的NaOH溶液,白色沉淀先增多后减少,但不完全溶解。
①原溶液中一定存在的离子有;一定不存在的离子有。
②补齐检验溶液中不能确定离子的操作:取少量滤液a,。
③写出第(3)个实验中白色沉淀减少过程中发生的离子反应方程式:。
④结合实验(3),你认为实验室制备 ,用可溶性铝盐和反应更佳(填化学式)。
①将四种盐分别加入试管中,并加水溶解,可观察到溶液颜色的情况为。
②向①的四支试管中分别加入稀盐酸,可观察到的现象为。
①取250 mL该混合溶液,加入过量盐酸,收集到标准状况下气体5.6 L;
②在操作①后的溶液中加入过量的NaOH溶液,过滤、洗涤、干燥得到白色沉淀5.8 g;
③在操作②后的溶液中加入过量的BaCl2溶液,过滤、洗涤、干燥得到白色沉淀23.3 g;
④在操作③后的溶液中加入过量的稀硝酸酸化的硝酸银溶液,产生大量的白色沉淀。
回答下列问题:
| 装置 | 现象 |
| | Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,液面上方出现浅棕色气体 Ⅲ.试管变热,溶液沸腾 |
①现象Ⅲ产生的原因。
②根据现象Ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
| 实验 | 内容 | 现象 |
| 实验1 | 将湿润KI—淀粉试纸置于空气中 | 试纸未变蓝 |
| 实验2 | 用湿润KI—淀粉试纸检验浅棕色气体 | 试纸变蓝 |
实验1、2说明反应生成了NO。
请用化学方程式解释气体变为浅棕色的原因。
| 装置 | 现象 |
| | Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,有刺激性气味 |
为确认:"刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
产生该刺激性气味气体的离子方程式是。
|
实验步骤与实验现象 |
实验结论 |
|
Ⅰ.观察溶液:无色透明 |
①原溶液中一定不含的离子是。 |
|
Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 |
②原溶液中一定不含的离子是,一定含有的离子是。 |
|
Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A |
③原溶液中还一定含有的离子是,生成沉淀A的离子方程式为。 |
|
Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B |
④白色沉淀B中一定含有,可能含有。 |

Y可能为(填化学式),B的组成为。
|
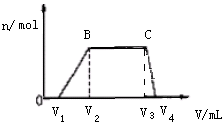
可能大量含有的阳离子 |
H+、Mg2+、Al3+、NH4+ |
|
可能大量含有的阴离子 |
Cl-、CO32- |
往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。(NH4++OH- =NH3·H2O)