| 目的 | 方案设计 | 现象和结论 | |
| A | 检验某无色溶液中是否含有NO | 取少量该溶液于试管中,加稀盐酸酸化,再加入FeCl2溶液 | 若溶液变黄色且试管上部产生红棕色气体,则该溶液中含有NO |
| B | 探究KI与FeCl3反应的限度 | 取5 mL 0.1 mol·L-1KI溶液于试管中,加入1 mL 0.1 mol·L-1 FeCl3溶液,充分反应后滴入5滴15% KSCN溶液 | 若溶液变血红色,则KI与FeCl3的反应有一定限度 |
| C | 判断某卤代烃中的卤素 | 取2 mL卤代烃样品于试管中,加入5 mL 20% KOH水溶液混合后加热,再滴加AgNO3溶液 | 若产生的沉淀为白色,则该卤代烃中含有氯元素 |
| D | 探究蔗糖在酸性水溶液中的稳定性 | 取2mL20%的蔗糖溶液于试管中,加入适量稀 H2SO4后水浴加热5 min;再加入适量新制Cu(OH)2悬浊液并加热 | 若没有生成砖红色沉淀 ,则蔗糖在酸性水溶液中稳定 |
选项 | 实验目的 | 实验操作及现象 | 实验结论 |
A | 检验硫酸厂周边空气是否含有SO2 | 用注射器多次抽取空气,慢慢注入盛有酸性KMnO4稀溶液的同一试管中,溶液不变色 | 空气中不含SO2 |
B | 证明CH3COOH是弱电解质 | 用pH计分别测量醋酸溶液和盐酸的pH,醋酸溶液的pH大 | CH3COOH是弱电解质 |
C | 探究淀粉的水解程度 | 向淀粉水解液中加入NaOH溶液调节溶液至碱性,并分成两份,向第一份中加入银氨溶液并水浴加热出现银镜;向第二份中滴加少量碘水,溶液变蓝色 | 淀粉部分水解 |
D | 探究卤素单质Cl2、Br2和I2的氧化性强弱 | 向NaBr溶液中通入过量氯气,溶液变橙色,再滴加淀粉KI溶液,溶液变蓝色 | 氧化性:Cl2>Br2>I2 |
|
选项 |
实验操作 |
实验现象 |
实验结论 |
|
A |
向溶液中滴加稀硫酸,并将产生的气体通过澄清石灰水 |
产生无色无味的气体,且石灰水变浑浊 |
该溶液中含 |
|
B |
向5mL 0.1mol·L-1NaOH溶液中滴加5mL0.01mol·L-1MgCl2溶液,然后再滴加5mL0.01mol·L-1CuCl2溶液 |
先产生白色沉淀,后产生蓝色沉淀 |
Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
|
C |
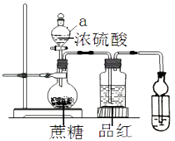
向蔗糖中加入适量浓硫酸并不断搅拌,同时将产生的气体通入品红溶液 |
蔗糖体积膨胀并变黑,品红溶液腿色 |
浓硫酸具有脱水性和氧化性 |
|
D |
向淀粉溶液中加入足量稀硫酸,加热一段时间后,加入少量Cu(OH)2悬浊液 |
产生砖红色沉淀 |
淀粉水解成葡萄糖 |
 B .
B .  C .
C . 
选项 | 实验 | 现象 | 结论 |
A | 向淀粉水解液中加入银氨溶液,加热 | 没有银镜产生 | 淀粉一定没有水解 |
B | 向 | 先产生白色沉淀,后白色沉淀变蓝 |
|
C | 向溴水中加入足量苯,振荡、静置 | 上层溶液颜色变浅 | 苯分子中化学键断裂 |
D | 将充满 | 热水中球泡颜色变深 |
|
实验 | 结论 | |
A | 将石蜡油加强热后产生的气体持续通入酸性 | 产生的气体中一定含有乙烯和丙烯 |
B | 用乙酸较长时间持续浸泡水壶中的水垢,水垢最终溶解消除 | 乙酸的酸性小于碳酸的酸性 |
C | 向油脂皂化后的溶液中滴入酚酞试液,溶液变红色 | 油脂皂化生成有碱 |
D | 蔗糖溶液在稀硫酸存在下水浴加热一段时间后,加氢氧化钠溶液调溶液至碱性,再加入银氨溶液混合加热,有光亮的银生成 | 蔗糖一定发生了水解 |
目的 | 方案设计 | 现象和结论 | |
A | 检验溶液中是否含有 | 取少量该溶液于试管中,先滴加 | 若沉淀不溶解,则说明溶液中含有 |
B | 探究淀粉水解程度 | 在试管中加入2mL淀粉溶液和适量稀硫酸,加热 | 若溶液中没有出现砖红色沉淀,则说明淀粉未水解 |
C | 验证乙醇脱水生成乙烯 | 向无水乙醇中加入浓硫酸,加热至170℃,将产生的气体通入溴水中 | 若溴水褪色,则有乙烯生成 |
D | 比较金属铝和氧化铝熔点的高低 | 用坩埚夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 铝箔熔化但不滴落,说明金属铝的熔点比氧化铝低 |
实验设计 | 实验目的 | |
A | 分别滴加淀粉溶液 | 鉴别 |
B | 用 | 证明酸性:盐酸>醋酸 |
C | 向 | 制备 |
D | 向反应后溶液中加入少量新制 | 检验蔗糖在稀酸催化下是否水解 |
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 先向某溶液中加入 | 开始时产生白色沉淀,后沉淀不溶解 | 原溶液中含有 |
| B | 向淀粉溶液中加适量20% | 溶液变蓝 | 淀粉未水解 |
| C | 将铁片插入稀硫酸中,一段时间后再往溶液中滴加少量 | 开始时有少量气泡产生,加入 | 形成Fe-Cu原电池,加快反应速率 |
| D | 将铜粉加入 | 溶液逐渐变蓝 | 还原性:Cu>Fe |

| 选项 | 实验操作和现象 | 结论 |
| A | 将一块镁片与一块铝片经电流表用导线连接,浸入NaOH溶液中,铝片逐渐溶解,电流表指针偏向镁片 | 铝片为负极 |
| B | 将 | |
| C | 将盐酸滴加到 | 非金属性:Cl>S |
| D | 往淀粉溶液中加入少量稀硫酸,加热。待溶液冷却后加入NaOH溶液调至碱性,再加入少量新制 | 淀粉完全水解 |
①前5分钟平均反应速率v(H2)=,H2的初始浓度是。
②下列能说明反应已达平衡状态的是(填序号)。
a.氢气的生成速率等于碘化氢的消耗速率
b.单位时间内断裂的H-H键数目与断裂的H–I键数目相等
c.c(H2):c(I2):c(HI)=1:1:2
d.2v(I2)正=v(HI)逆
e.反应混合体系的颜色不再发生变化
已知:“碘钟实验”的总反应的离子方程式为:H2O2+2 +2H+=
+2H2O,反应分两步进行:
反应A:…...
反应B:I2+2 =2I-+
①反应A的离子方程式是。对于总反应,I-的作用是。
②为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ。(溶液浓度均为0.01mol•L-1)
| H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | KI溶液(含淀粉) | H2O | |
| 实验Ⅰ | 5 | 4 | 8 | 3 | 0 |
| 实验Ⅱ | 5 | 2 | x | Y | z |
溶液从混合时的无色变为蓝色的时间:实验I是30min、实验II是40min。实验II中,x、y、z所对应的数值分别是;对比实验I、II、可得出的实验结论是。
A;
B。
A.菠菜B.花生油 C.瘦肉D.西瓜
编号 | 操作 | 现象 |
1 | 加入碘水 | 溶液变成蓝色 |
2 | 加入银氨溶液,水浴加热 | 未出现银镜 |
3 | 加入碘水 | 溶液变成蓝色 |
4 | 加入银氨溶液,水浴加热 | 未出现银镜 |
结合试管1、2中的现象,得出的结论是这两支试管中淀粉水解(填“没有”“部分”或“全部”).结合试管3、4中的现象,不能得出“这两支试管中淀粉没有水解”的结论,理由是.
