4.
(2024高二上·成都期末)
某温度下,向10mL0.1mol·L
−1Pb(NO
3)
2溶液中滴加0.1mol·L
−1Na
2S溶液,溶液中-lgc(Pb
2+)与滴加的Na
2S溶液体积V的关系如图所示(忽略体积变化)。已知:K
sp(PbS)<K
sp(FeS)。下列判断正确的是( )

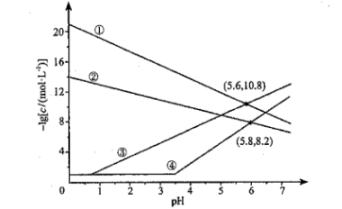
A . a、b、c三点中Ksp(PbS)从大到小的顺序为:a>b>c
B . b点:c(Pb2+)<c(S2−)
C . c点:2c(Pb2+)+c(H+)=c(NO3−)+c(OH−)
D . 其他条件相同时,若将Pb(NO3)2溶液换成同浓度、同体积的Fe(NO3)2溶液,图中-lgc(Pb2+)换成-lgc(Fe2+),则b点会沿虚线向下移动

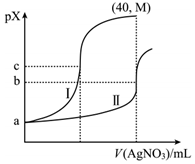
溶液滴入2 mL 0.1 mol/L NaCl溶液中,观察到生成白色沉淀。

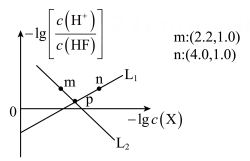
为微溶于水,溶于盐酸,不溶于氢氟酸、乙醇和丙酮的固体。


