
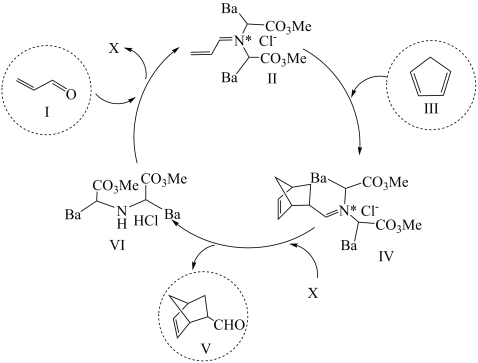
 , 则产物为
, 则产物为
| t/min | 0 | 20 | 40 | 60 | 80 |
| c/(mol·L-1) | 0.80 | 0.40 | 0.20 | 0.10 | 0.050 |
下列说法错误的是( )
| 选项 | 目的 | 实验 |
| A | 制取较高浓度的次氯酸溶液 | 将Cl2通入碳酸钠溶液中 |
| B | 加快氧气的生成速率 | 在过氧化氢溶液中加入少量MnO2 |
| C | 除去乙酸乙酯中的少量乙酸 | 加入饱和碳酸钠溶液洗涤、分液 |
| D | 制备少量二氧化硫气体 | 向饱和亚硫酸钠溶液中滴加浓硫酸 |
 为该反应的催化剂
C . 该反应中存在极性键的断裂和非极性键的形成
D . 根据
为该反应的催化剂
C . 该反应中存在极性键的断裂和非极性键的形成
D . 根据
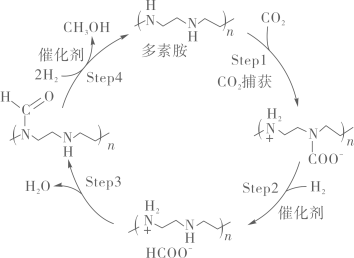

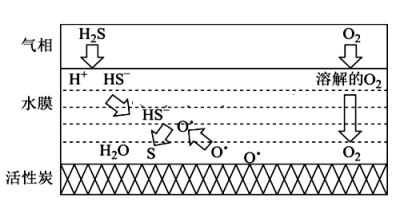
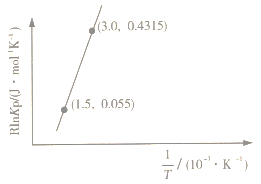
已知:RlnKp=-+C(R、C均为常数)。
下列说法错误的是( )



①
②
③
计算反应④的
;
⑤
⑥
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S()随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是,理由是;

苯乙烯聚合有多种方法,其中一种方法的关键步骤是某(Ⅰ)的配合物促进
(引发剂,X表示卤素)生成自由基
, 实现苯乙烯可控聚合。
反应i:CO2(g)+4H2(g)CH4(g)+2H2O(g) ΔH1
反应ii:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH2=-49kJ·mol-1
化学键 | H-H | O-H | C-H | C=O |
能量/kJ | 436 | 463 | 413 | 803 |
①为了提高CH3OH产率可以采取的措施有(任写两项措施)。
②图1中能表示该反应的平衡常数的对数lnK与(T表示温度)之间的变化关系的曲线是(选填“m”或“n”)。

③测得在相同时间内,不同温度下的H2转化率如图2所示,v(a)逆v(c)逆(选填“>”“<”或“=”);T2温度下该反应的平衡常数K值为(保留两位小数)。


①曲线a的进料浓度比c(CO2):c(H2)为。
②条件X是(选填“温度”或“压强”),依据是。

①阴极的电极反应为。
②试从图4分析,采用BiIn合金催化剂既优于单金属Bi催化剂,又优于单金属In催化剂的原因。
CO2(g)+2H2(g)
CH4(g)+H2O(g),ΔH总Kp总 , 该反应分两步完成,反应过程如下:
①CO2(g)+H2(g)CO(g)+H2O(g),ΔH1Kp1
②CO(g)+H2(g)CO2(g)+
CH4(g),ΔH2Kp2
回答下列问题:

对比上述两种催化剂的催化性能,工业上应选择的催化剂是,使用的合适温度为。

则T1温度下Kp1=,从图像分析反应①的ΔH10(填“>”“<”或“=”)。

①由如图可知用Al/Cu二元金属复合材料去除水体中硝酸盐效果明显优于铝粉,可能原因是。
②实验发现Al/Cu二元金属复合材料中Cu负载量过高也不利于硝酸盐的去除,可能原因是。

①使用Al/Cu二元金属复合材料,可将水体中硝酸盐转化为铵盐,该转化的机理可描述为: H+吸附在Cu表面并得电子生成强还原性的吸附氢H(ads),, NH3与H+结合为进入溶液。
②引入Pd的Al/Cu/Pd三元金属复合材料,硝酸盐转化为N2选择性明显提高,可能原因是
③其他条件相同时,Al/Cu/Pd 三元金属复合材料去除水体中硝酸盐的效果与溶液pH关系如图所示。水体pH在4至6范围内,随pH增大硝酸盐去除率降低的可能原因是;水体pH在8.5至10范围内,随pH增大硝酸盐去除率升高的可能原因是。

Ⅰ. 2H2(g)+O2(g)
2H2O(g) ΔH1= -483.6 kJ·mol-1
Ⅱ.N2(g)+O2(g) 2NO(g) ΔH2 = +180.5 kJ·mol-1
Ⅲ.2H2(g)+ 2NO(g) N2(g)+ 2H2O(g) ΔH3

图1
①下列能够说明该反应已达到化学平衡状态的是
A.2v逆 (NO)=v 正(N2)
B.混合气体的密度不再变化
C.容器内总压强不再变化
D.混合气体的平均相对分子质量不再变化
②使用催化剂乙、温度高于350℃时,NO 转化率降低的原因可能是。
③研究表明该反应v= kcm(H2)c2(NO),其中k为速率常数,与温度、活化能有关。T1℃的初始速率为v0 , 当H2转化率为50%时,反应速率为 ,由此可知m=。设此时反应的活化能为Ea',不同温度T1、T2条件下对应的速率常数分别为k1、k2 , 存在关系:
(R为常数)。据此推测:活化能越大,升高温度,速率常数增大倍数。 (填“越大”“越小”或“不变”)

图2
①物质的量分数为: 75%的H2和25%的N2所对应的曲线是。 (填“a”或“b”)
②M点时,N2的转化率为;该 反应的压强平衡常数Kp= (MPa)-2(用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(ⅰ)CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
(ⅱ)CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.1 kJ/mol
由CO也能直接加氢合成甲醇:(iii) 2H2(g)+CO(g) CH3OH(g) △H

下列分析正确的是_______。

①使用催化剂M时,逆反应的活化能为kJ/mol。
②催化剂N对应曲线是图(b)中的(填“Ⅰ”或“Ⅱ”)

①三个容器中,甲醇的生成速率达峰值后均随温度升高而下降的原因是。
②结合研究目的,参照图中三条曲线,你可得出的结论是(写一条)。
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH2=-2600 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH3=-572 kJ/mol
则2CH4(g)=C2H2(g)+3H2(g)ΔH=kJ/mol
 分别表示CH4、CH2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示,从吸附到解吸的过程中,能量状态最高的是(填标号)。
分别表示CH4、CH2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图所示,从吸附到解吸的过程中,能量状态最高的是(填标号)。 
②在恒容密闭容器中充入amol甲烷,测得单位时间内在固体催、化剂表面CH4的转化率[α(CH4)]与温度(t℃)的关系如图所示,t0℃后CH4的转化率突减的原因可能是。


①T℃时,化学反应2CH4 (g)=C2H2(g)+3H2(g)的压强平衡常数K=Pa2。
②在某温度下,向VL恒容密闭容器中充入0.12mol CH4只发生反应2CH4(g)=C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4)。CH4的平衡转化率为(结果保留两位有效数字)。
I.CH4(g)+H2O(g)→CO(g)+3H2(g) ΔH1=+206kJ·mol-1;
II.CO(g)+H2O(g)→CO2(g)+H2(g) ΔH2=-41kJ·mol-1;
在一体积可变的密闭容器中,加入一定量的CH4和H2O(g)发生水蒸汽重整反应。
①压强为P0kPa时,分别在加CaO和不加CaO时,平衡体系H2的物质的量随温度变化如图所示。温度低于700℃时,加入CaO可明显提高混合气中H2的量,原因是

②500℃时,反应相同时间后测得CH4的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(G)(填“>”“<”或“=”)c(E)。

步骤1:向试管中加入4mL淀粉溶液,再加入少量稀硫酸,加热4分钟,冷却后将溶液分装在两支试管中;
步骤2:向一支试管中滴加几滴碘水,观察现象;
步骤3:向另一支试管中先加入烧碱溶液中和,再加入银氨溶液,水浴加热煮沸,观察现象。
下列说法错误的是( )

反应I:CO(g)+2H2(g)CH3OH(g) ΔH1<0
反应II:2CO(g)+4H2(g)C2H5OH(g)+H2O(g) ΔH2<0
反应III:2CO2(g)+6H2(g)C2H5OH(g)+3H2O(g) ΔH3<0
反应IV:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH4<0
反应V:2CH3OH(g)C2H5OH(g)+H2O(g) ΔH5
回答下列问题:
已知:CH3OH的选择性=×100%;C2H5OH的选择性=
×100%

①图甲中x3(填“大于”“小于”或“等于”),其原因是。
②Q点对应的体系中n(CH3OH)=mol;此时,H2转化了4mol,则反应2CH3OH(g)C2H5OH(g)+H2O(g)的平衡常数Kp=(Kp为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留两位有效数字)。

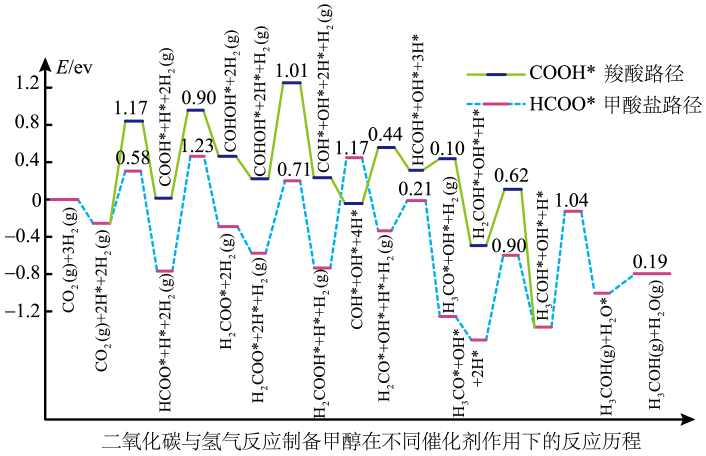
①据图,CO和CO2相比,(填化学式)更稳定。
②吸附在催化剂表面上的物种用*标注,图中第一步反应为CO2+e-+H+=*COOH,则第二步反应为。
![]()
;
。
则。

①起始时投入的苯酚和氢气的物质的量之比为。
②A、B、C、D四点对应的正反应速率、
、
、
的大小关系为。
③温度低于400℃时,和苯酚的转化率随温度升高而增大的原因是。
④已知 , V代表体积;n代表气体物质的量;T代表温度;R是摩尔气体常数,单位是
。若初始时向容器中充入的苯酚为1mol,则反应从起始进行到A点,其平均反应速率
;当反应温度为500℃时,反应达到平衡后,
。(
表示用分压代替浓度计算的平衡常数,结果用含R的代数式表示)