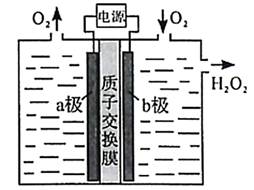




下列说法错误的是






下列有关说法正确的是( )

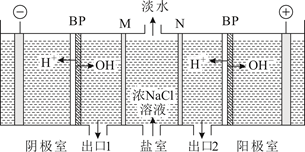



选项 | X极 | 实验前U形管中液体 | 通电后现象及结论 |
A | 正极 | CuCl2溶液 | b管中有气体逸出 |
B | 负极 | H2SO4溶液 | 溶液pH降低 |
C | 正极 | NaCl溶液 | U形管两端滴入酚酞后,b管中溶液呈红色 |
D | 负极 | AgNO3溶液 | a管中电极反应式是2H2O-4e-=O2↑+4H+ |

①写出400~600 ℃范围内分解反应的化学方程式:。
②与CaCO3热分解制备的CaO相比,CaC2O4·H2O热分解制备的CaO具有更好的CO2捕集性能,其原因是。

①写出阴极CO2还原为HCOO−的电极反应式:。
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是。
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH =41.2 kJ·mol−1
反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH =﹣122.5 kJ·mol−1
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:

CH3OCH3的选择性= ×100%
①温度高于300 ℃,CO2平衡转化率随温度升高而上升的原因是。
②220 ℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施有。
温度/℃ | 压强/MPa | 氨的平衡含量 |
200 | 10 | 81.5% |
550 | 10 | 8.25% |
①该反应为(填“吸热”或“放热”)反应。
②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是。

①曲线a对应的温度是。
②M、N、Q点平衡常数K的大小关系是。

4NH3(g)+3O2(g)2N2(g)+6H2O(g)ΔH=-1268kJ·mol-1
2NO(g)N2(g)+O2(g)ΔH=-180.5kJ·mol-1
请写出NH3转化为NO的热化学方程式。

资料:金属离子沉淀的pH
金属离子 | Fe3+ | Fe2+ | Co2+ | Mn2+ |
开始沉淀 | 1.5 | 6.3 | 7.4 | 7.6 |
完全沉淀 | 2.8 | 8.3 | 9.4 | 10.2 |

i.称取10.0g废渣,加酸将锰元素全部溶出成Mn2+ , 过滤,将滤液定容于100mL容量瓶中。
ii.取25.00mL溶液于锥形瓶中,加入少量催化剂和过量(NH4)2S2O8(过氧硫酸铵)溶液,加热、充分反应后,煮沸溶液使过量的(NH4)2S2O8分解。
iii.加入指示剂,用bmol/L(NH4)2Fe(SO4)2溶液滴定。滴定至终点时消耗(NH4)2Fe(SO4)2溶液的体积为cmL, 重新变成Mn2+。
①写出下面补全的步骤ⅱ中反应的离子方程式:。
2Mn2++ + ▲ =
+ ▲ + ▲ 。
②废渣中锰元素的质量分数为。

S2--2e-=S (n-1)S+S2-=S

①写出阴极的电极反应方程式。
②电解后阳极区溶液用稀硫酸酸化得到硫单质,其离子方程式为。
①用Fe2(SO4)3吸收液脱除H2S的原理经历以下三步:
第一步:H2S(g)H2S(aq)
第二步:H2SH++HS-
第三步:HS-+2Fe3+=S↓+2Fe2++H+
一定条件下,不同Fe3+浓度溶液及该溶液起始pH与脱硫率的关系如图所示。当Fe3+浓度大于10 g·L-1时,随着Fe3+浓度增大,脱硫率逐渐降低。其原因是。

②反应后的溶液在硫杆菌作用下进行再生的反应为:4FeSO4+O2+2H2SO42Fe2(SO4)3+2H2O。反应相同时间后,溶液中Fe2+的氧化速率与温度的关系如图所示。温度超过30℃后,随着温度升高,Fe2+的氧化速率下降的原因是。

①适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是。
②若水膜过厚,H2S的氧化去除率减小的原因是。

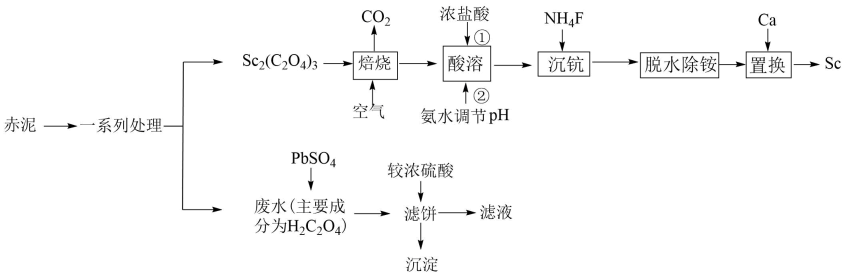
已知:25℃时,部分物质的相关数据如表。
Ksp(PbSO4) | Ksp(PbC2O4) | Ka1(H2C2O4) | Ka2(H2C2O4) |
2.0×10-8 | 5.0×10-10 | 6.0×10-2 | 6.25×10-5 |



△H=(用图中字母表示)。该反应在(填“高温”“低温”或“任意温度”)条件下自发进行。
①2NO(g) N2O2(g)(快)
②N2O2(g) + H2(g) N2O(g) + H2O(g)(慢)
③N2O(g)+H2(g) N2(g)+ H2O(g)(快)
下列各反应的活化能最大的是_______(填标号)。

①其中T1℃的实验结果所对应的曲线是(填标号);当曲线X、Y、Z达到相同的NO平衡转化率时,对应的反应温度与投料比的规律是。
②T2℃时,若充入H2、NO分别为5mol、2mol,容器内的压强为p0Pa,反应进行到5min时达平衡,0~5min内NO的平均反应速率为。该反应的平衡常数Kp=Pa-1 (用平衡分压代替平衡浓度写出计算表达式,分压=总压×物质的量分数)。

①
②
③。

①实际生产选择图中A点的反应条件,不选择B、C点的理由分别是。
②在温度T℃下,向某恒容密闭容器中充入 、
和
,起始时压强为p,进行反应
。平衡时,
转化率为80%,则平衡时
分压为(用含p的代数式表示,下同),平衡常数
(以分压代替浓度计算,分压=总压×物质的量分数)。

①为使电池持续工作,电解质溶液中的(填离子符号)从(填“甲”或“乙”,下同)室通过离子交换膜移向室。
②起始时,稀硫酸中含 和
,当甲电极消耗
时,甲、乙两室中
与
的总物质的量之比为。(两电极的产物均留在溶液中,忽略水的电离)
Ⅰ.
Ⅱ.
回答下列问题:


①该条件下,N2(g)+3H2(g)⇌2NH3(g) △H=。
②写出一条既能加快反应速率又能提高N2平衡转化率的措施。

反应原理为:NO(g)+NO2(g)+2NH3(g)⇌2N2(g)+3H2O(g)。
下列说法正确的是_______(填序号)。

①电解时双极膜中的H2O解离为H+和OH- , H+向室(填“a”或“b”)移动。
②写出阳极的电极反应式。
|
序号 |
实验装置 |
实验操作 |
实验现象 |
|
A |
| 向滤液中放入Mg条 | ⅰ.滤液澄清透明,用激光照射有丁达尔现象。 ⅱ.放入Mg条后,立即有无色气泡产生,气体可燃,滤液中出现白色浑浊,ⅲ.一段时间后开始出现棕褐色浑浊物。Mg条表面也逐渐变为棕褐色。产生气泡的速率变缓慢 |
已知:①AgOH不稳定,立即分解为Ag2O (棕褐色或棕黑色),Ag粉为黑色;
②AgCl、Ag2O可溶于浓氨水生成 [Ag(NH3)2]+(银氨溶液),Mg、Ag不溶于浓氨水。
①设计实验检验Ag:取实验A中表面变为棕褐色的Mg条于试管中,向其中加入足量稀盐酸,反应结束后,继续加入浓硝酸,产生棕色气体和白色不溶物。用离子方程式表示棕褐色固体中产生Ag的原因:。实验中加入稀盐酸的目的:。
②设计检验棕褐色物质中有Ag2O,实验方案是:取实验A中表面变为棕褐色的Mg条用蒸馏水洗净后,加入(填化学式)中浸泡,取上层清液于葡萄糖溶液中,水浴加热,若有(填实验现象),则证明Ag2O存在。
|
装置 |
步骤 |
电压表读数 |
|
| ⅰ.如图连接装置并加入试剂,闭合K | a |
| ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | |
| ⅲ.再向B中投入一定量NaCl(s) | c | |
| ⅳ.重复ⅰ,再向B中加入与iii等量NaCl(s) | d |
已知:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
①电压表读数a>b,其原因是。
②综合实验现象能说明AgI转化为AgCl,则a、b、c三者的大小关系为。